Презентація на тему:
"Каменный уголь"
Завантажити презентацію
"Каменный уголь"
Завантажити презентаціюПрезентація по слайдам:
ТЕОРИЯ ПРОИСХОЖДЕНИЯ Уголь – это остатки растений, погибших многие миллионы лет назад, гниение которых было прервано в результате прекращения доступа воздуха.
растительные останки торф бурый уголь каменный уголь антрацит графит. УГЛЕФИЦИРОВАНИЕ Е М Т А М О Р Ф И З М
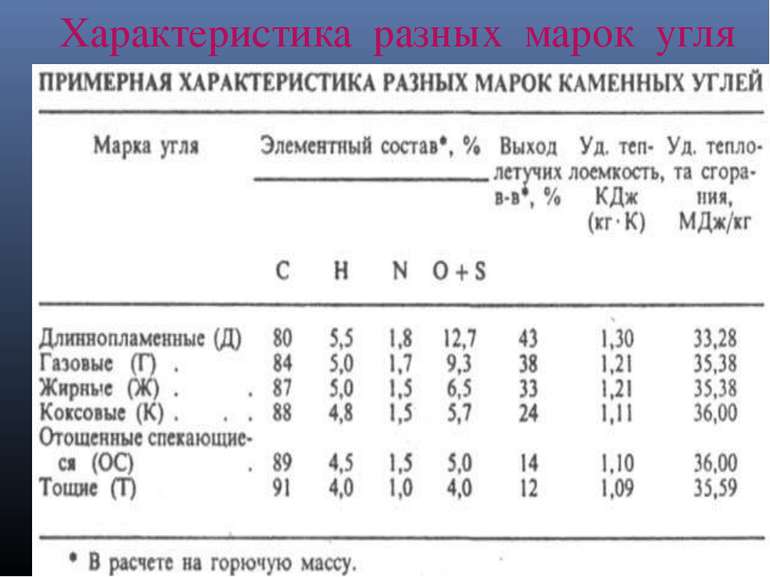
Характерные физические свойства каменного угля: - содержание углерода (С,%) - 75-97; - плотность (г/см3) – 1,28-1,53; - механическая прочность (кг/см2) – 40-300; - удельная теплоемкость С (Ккал/г град) – 026-032; - коэффициент преломления света – 1,82-2,04.
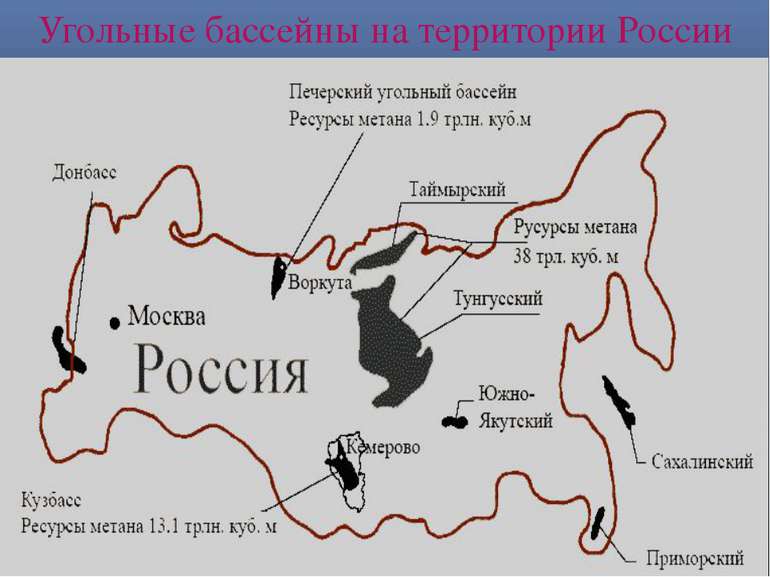
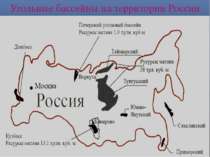
СОСТАВ И ВАЖНЕЙШИЕ МЕСТОРОЖДЕНИЯ Состав каменного угля очень сложен: в нем содержатся как органические, так и неорганические вещества. Запасы угля на нашей планете значительно превышают запасы нефти. Небольшую его часть используют как топливо, в основном же он удовлетворяет нужды коксохимического производства. Переработка каменного угля в настоящее время становится одним из основных направлений в химической промышленности. Каменный уголь представляет собой полезное ископаемое, которое образовалось миллионы лет назад из отмерших остатков растений в результате сложных процессов.
Состав Каменного угля Состав каменного угля очень сложен: в нем содержатся как органические, так и неорганические вещества.
По признакам различают: блестящие (витрен), полублестящие (кларен), матовые (дюрен), волокнистые (фюзен). Эти составляющие чаще всего располагаются слоями, придавая каменным углям полосчатую структуру.
Составные части каменного угля Основная - горючая, или органическая, масса угля (ОМУ), влага и минер. включения, образующие при сжигании золу; Зольность каменных углей составляет 5-30% по массе и более; Главные составляющие золы: оксиды Si, Fe и Аl, редкие и рассеянные элементы (Ge, V, W, Ti и т.д.), а также драгоценные металлы (Au, Ag). Горючая масса содержит С, Н, N, О и S, входящую также в состав минер.
Химический состав По химическому составу каменный уголь представляет смесь высокомолекулярных полициклических ароматических соединений с высокой массовой долей углерода, а также воды и летучих веществ с небольшими количествами минеральных примесей, при сжигании угля образующих золу. Ископаемые угли отличаются друг от друга соотношением слагающих их компонентов, что определяет их теплоту сгорания. Ряд органических соединений, входящие в состав каменного угля, обладает канцерогенными свойствами.
Зола Главные составляющие золы: оксиды Si, Fe и Аl, редкие и рассеянные элементы (Ge, V, W, Ti и т.д.), а также драгоценные металлы (Au, Ag) Горючая масса содержит С, Н, N, О и S, входящую также в состав минеральной части.
ОМУ Широкое распространение получили представления о гибридном характере мол. структуры, состоящей из пространственных, плоскостных и линейных фрагментов. Последние включают преим. макроалифатич. Радикалы и О-, N- и S- содержащие функциональные группы (см. также Гидрогенизация угля).
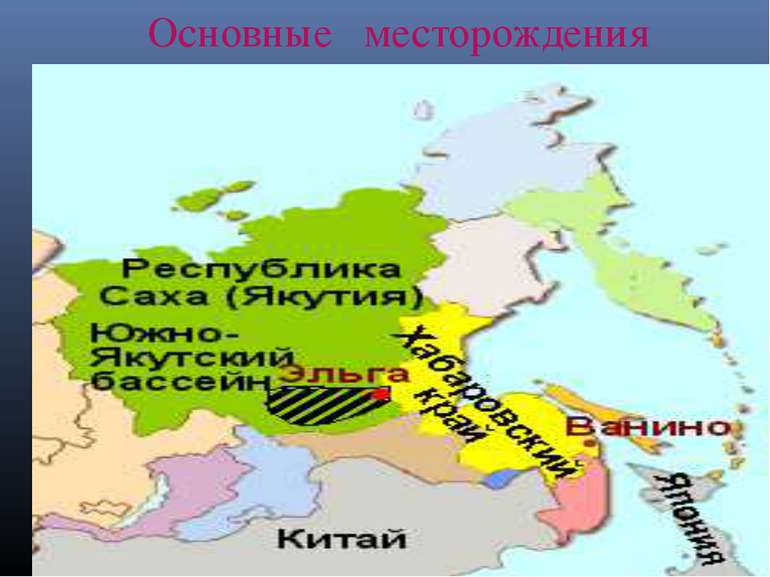
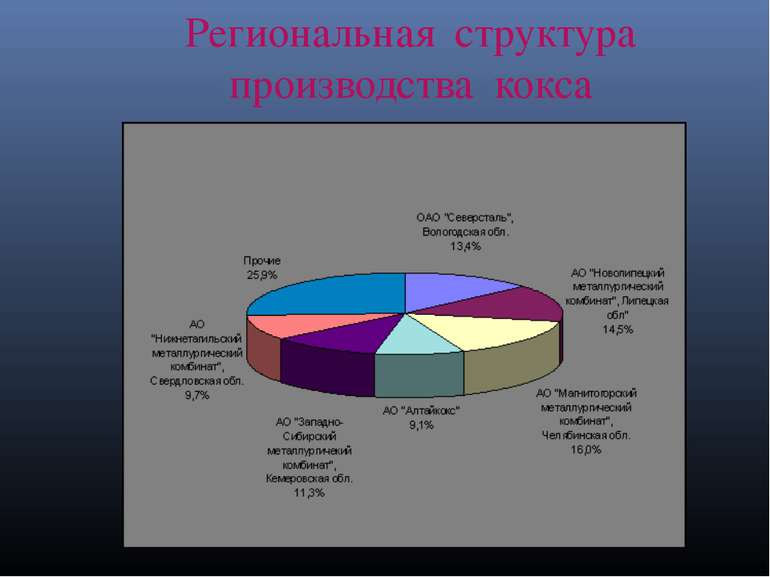
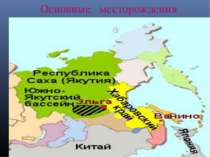
Основные месторождения Эльгинское месторождение (Саха). Наиболее перспективный объект для открытой разработки — находится на юго-востоке Республики Саха. Площадь месторождения 246 км2. Месторождение представляет собой пологую брахисинклинальную асимметричную складку. Угленосны отложения верхней юры и нижнего мела. Основные угольные пласты приурочены к отложениям нерюнгринской (6 пластов мощностью 0,7-17 м) и ундыктанской (18 пластов мощностью также 0,7-17 м) свит. Угли в основном полублестящие линзовидно-полосчатые с очень высоким содержанием наиболее ценного компонента — витринита (78-98 %). По степени метаморфизма угли относятся к III (жирной) стадии. Марка угля Ж, группа 2Ж. Угли средне- и высокозольные (15—24 %), малосернистые (0,2 %), малофосфористые (0,01 %), хорошо спекающиеся (Y = 28—37 мм), с высокой теплотой сгорания (28 МДж/кг). Месторождение представлено мощными (до 17 метров) пологими пластами с перекрывающими отложениями небольшой мощности (коэффициент вскрыши — около 3 куб м на тонну рядового угля), что очень выгодно для организации добычи открытым способом. Элегестское месторождение (Тува) обладает запасами около 1 млрд т коксующегося угля дефицитной марки «Ж» (общий объем запасов оценивается в 20 млрд т). 80 % запасов находится в одном пласте толщиной 6,4 м (лучшие шахты Кузбасса работают в пластах толщиной 2-3 м, в Воркуте уголь добывают из пластов тоньше 1 м). После выхода на проектную мощность к 2012 году на Элегесте ожидается -добыча 12 млн т угля ежегодно. Лицензия на разработку элегестских углей принадлежит Енисейской промышленной компании, которая входит в структуру «Объединенной промышленной корпорации» (ОПК). Правительственная комиссия по инвестиционным проектам РФ 22 марта 2007 года одобрила реализацию проектов по строительству железнодорожной линии «Кызыл-Курагино» в увязке с освоением минерально-сырьевой базы Республики Тува.
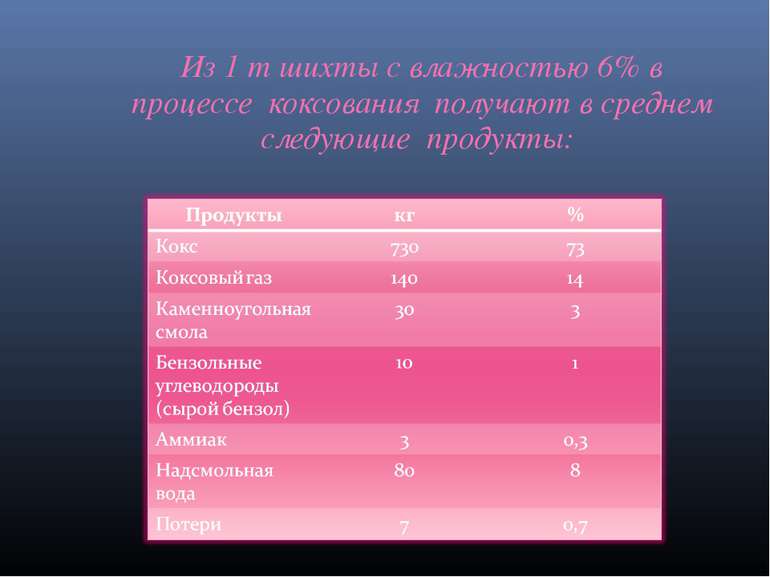
ВАЖНЕЙШИЕ ПРОДУКТЫ, ПОЛУЧАЕМЫЕ ПРИ ПЕРЕРАБОТКЕ УГЛЯ Из угля при химической переработке получают до 300 наименований разнообразных продуктов. Получают высокоуглеродистые углеграфитовые материалы, горный воск, пластические массы, синтетическое, жидкое и газообразное высоко- калорийное топливо. А так же ароматические продукты путём гидрогенизации и высоко азотистые кислоты для удобрений.
Кокс и побочные продукты каменного угля Батарея коксовых печей со стороны коксовыталкивателя Кокс - серое, чуть серебристое, пористое и очень твердое вещество, более чем на 96% состоящее из углерода и получаемое при нагревании каменного угля или нефтяных пеков без доступа воздуха при 950-1050°С. Процесс получения- кокса в результате переработки природных топлив называется коксованием. кокс сухой 78,0 смола. 3,5 бензол 1,0 аммиак 0,3 коксовый газ сухой 16,0 пирогенетическая влага 1,2 Итого 100,0
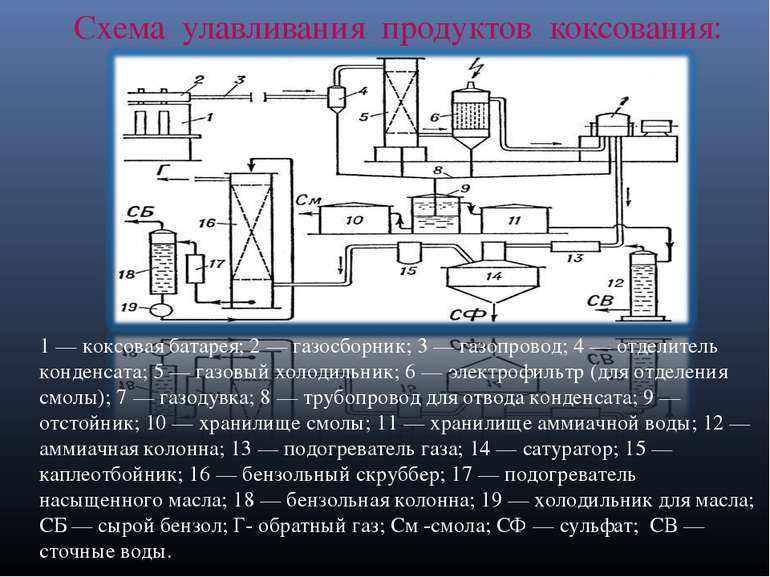
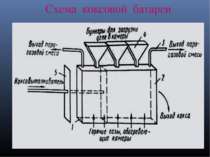
Схема улавливания продуктов коксования: 1 — коксовая батарея; 2 — газосборник; 3 — газопровод; 4 — отделитель конденсата; 5 — газовый холодильник; 6 — электрофильтр (для отделения смолы); 7 — газодувка; 8 — трубопровод для отвода конденсата; 9 — отстойник; 10 — хранилище смолы; 11 — хранилище аммиачной воды; 12 — аммиачная колонна; 13 — подогреватель газа; 14 — сатуратор; 15 — каплеотбойник; 16 — бензольный скруббер; 17 — подогреватель насыщенного масла; 18 — бензольная колонна; 19 — холодильник для масла; СБ — сырой бензол; Г- обратный газ; См -смола; СФ — сульфат; СВ — сточные воды.
В доменной печи кокс сгорает и образуется оксид углерода (IV): С + О2 = СО2 + Q, который взаимодействует с раскаленным коксом с образованием оксида углерода (II): С + СO2 = 2CO – Q Оксид углерода (II) и является восстановителем железа, сначала из оксида железа (III) образуется оксид железа (II, III), затем оксид железа (II) и, наконец, железо: 3Fe2O3 + CO = 2Fe3O4 + CO2 + Q Fe3O4 + CO = 3FeO + CO2 – Q FeO + CO = Fe + CO2 + Q Доменная печь
Кроме кокса при сухой перегонке каменного угля образуются также летучие продукты, при охлаждении которых до 25-75 С образуется каменноугольная смола, аммиачная вода и газообразные продукты. Каменноугольная смола подвергается фракционной перегонке, в результате чего получают несколько фракций: - легкое масло (температура кипения до 170 С) в нем содержится ароматические углеводороды (бензол, толуол, кислоты и др. вещества); - среднее масло (температура кипения 170-230 С). Это фенолы, нафталин; - тяжелое масло (температура кипения 230-270 С). Это нафталин и его гомологи - антраценовое масло – антрацен, фенатрен и др.
В состав газообразных продуктов (коксового газа) входят: Бензол; Толуол; Ксиолы; Фенол; Аммиак и др. вещ. Из коксового газа после очистки от аммиака, сероводорода и цианистых соединений извлекают сырой бензол, из которого выделяют отдельные углеводороды и ряд других ценных веществ.
Продукты, получаемые при обработке коксового газа Из коксового газа углеводороды извлекают промывкой в скрубберах жидкими поглотительными маслами. После отгонки от масла, разгонки из фракции, очистки и повторной ректификации получают чистые товарные продукты, как-то: бензол, толуол, ксилолы и др. Из непредельных соединений, содержащихся в сыром бензоле, получают кумароновые смолы, использующиеся для производства лаков, красок, линолеума и в резиновой промышленности. Перспективным сырьем является также циклопентадиен, который также получают из каменного угля. Каменный уголь – сырье для получения нафталина и других индивидуальных ароматических углеводородов. Важнейшими продуктами переработки являются пиридиновые основания и фенолы.
Основная проблема при использовании каменного угля – огромное количество выбросов, в частности парниковых газов. Выбрасывается около 44% от всех выбросов СО2. В течение года выброс происходит неравномерно.
По уровню производственного травматизма угольная промышленность занимает в производственной сфере печальное лидирующее положение Для угольной отрасли характерен низкий уровень санитарно-гигиенической безопасности условий труда.
Серьезные экологические проблемы возникают в районах размещения золошлаковых отходов угольных ТЭС и при хранении.
КОКСОВАНИЕ Коксование — процесс переработки жидкого и твёрдого топлива нагреванием без доступа воздуха. При разложении топлива образуются твёрдый продукт — кокс и летучие продукты. Кокс - серое, чуть серебристое, пористое и очень твердое вещество, более чем на 96% состоящее из углерода и получаемое при нагревании каменного угля или нефтяных пеков без доступа воздуха при 950-1050°С.
Этот широко распространённый технологический процесс состоит из 3 стадий: 1) подготовка к коксованию; 2)собственно коксование; 3)улавливание и переработка летучих продуктов.
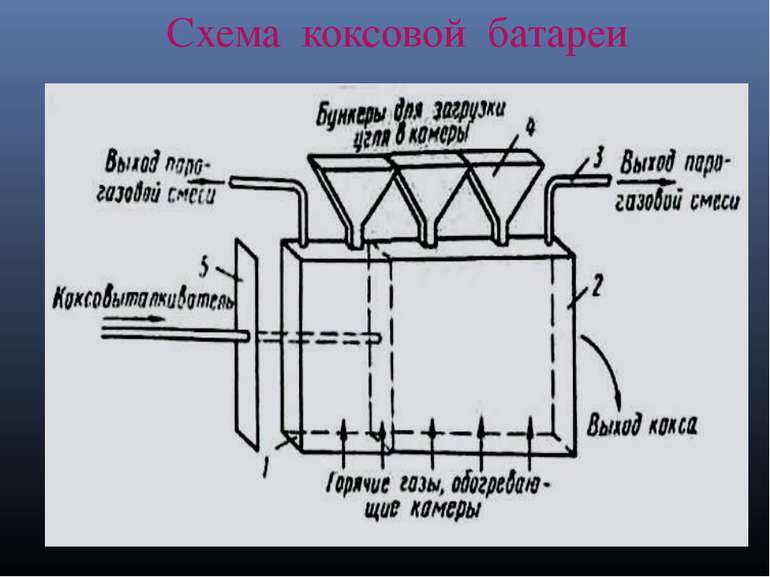
Стадии коксования Подготовка включает обогащение, измельчение до зёрен размером около 3 мм, смешение нескольких сортов угля, сушка полученной «шихты». Для коксования шихту загружают в коксовую печь. Каналы боковых простенков печей обогреваются продуктами сгорания газов. Продолжительность нагрева составляет 14-16 часов. Температура процесса — 900—1050 °C. Полученный кокс (75-78 % от массы исходного угля) в виде «коксового пирога» (спёкшейся в пласт массы) — выталкивается «коксовыталкивателями» в железнодорожные вагоны, в которых охлаждается («тушится») водой или инертным газом (азотом). Парогазовая смесь выделяющихся летучи продуктов (до 25 % от массы угля) отводится через газосборник для улавливания и переработки. Для разделения летучие продукты охлаждают впрыскиванием распыленной воды (от 700 °C до 80 °C) — при этом из паровой фазы выделяется большая часть смол, дальнейшее охлаждение парогазовой смеси проводят в кожухотрубчатых холодильниках (до 25-35 °С). Конденсаты объединяют и отстаиванием выделяют надсмольную воду и каменноугольную смолу. Затем сырой коксовый газ последовательно очищают от NH3 и H2S, промывают поглотительным маслом , серной кислотой.
Схема коксования: Схема коксования: 1 – коксовая батарея; 2 – сборный канал продуктов горения; 3 – газопровод; 4 – отделитель конденсата; 5 – газовый холодильник; 6 – электрофильтр; 7 – газодувка; 8 – трубопровод для отвода конденсата; 9 – отстойник; 10 – хранилище смолы; 11 – хранилище аммиачной воды; 12 – аммиачная колонна; 13 – сатуратор; 14 – бензольный скруббер; 15 – бензольная колонка.
Способы очистки коксового газа от H2S Сухой Мокрый Сухая очистка коксового газа от сероводорода основана на применении твердых поглотителей – гидроксида железа (III) Fe(OH)3 (болотной руды) и активиро-ванного угля. Этот метод обеспечивает глубокую (тонкую) очистку и служит вспомогательным при мокрой очистке. Он может использоваться для доочистки газа, который передается на дальнее расстояние. 1. Методы, основанные на получении концентрированного газообразного H2S с последующим окислением его в серу или серную кислоту: H2S + ОН– ⇔ HS– + Н2О H2S + 2ОН– ⇔ S–2 + 2Н2О 2. Методы основаны на непосредственном окислении H2S, содержащегося в коксовом газе, в элементарную серу: 2H2S + О2 = 2S + 2Н2О 3. Методы, основанные на одновременном улавливании аммиака и сероводорода.
Образование HСN при коксовании При коксовании каменных углей образуются цианистые соединения: дициан (СN)2 и цианистый водород НСN или цианистоводородная кислота (синильная кислота). Содержание дициана в коксовом газе невелико, поэтому содержащиеся цианистые соединения в газе относят главным образом к цианистому водороду. В цианистый водород переходит до 2% азота, содержащегося в угле. Цианистый водород – продукт вторичных реакций, протекающих между аммиаком, углеродом и углеводородами. Одной из таких реакций является взаимодействие аммиака с углеродом кокса: NH3 + С —→ + Н2. С повышением температуры коксования, снижением влажности шихты и увеличением высоты коксовой камеры выход цианистого водорода повышается.
Очистка коксового газа от HCN Сухой Мокрый Сухая очистка газа от цианистого водорода болотной рудой – наиболее простой метод и осуществляется попутно с поглощением сероводорода. Степень извлечения цианистого водорода болотной рудой достаточно высока (85–95%). В результате некоторых реакций цианистый водород оказывается связанным в болотной руде в виде Fе(СN)2 и главным образом в виде Fе7(СN)18, однако эти соединения не выделяются из поглотительной массы и полностью теряются. 1. Полисульфидная очистка (полусильфидом натрия) с получением двухводной соли роданистого натрия. Степень очистки - 95%: HСN + Nа2СO3 = NаСN + NаНСО3 NаСN + Na2Sn = NaСNS + Nа2Sn-1; 2. Полисульфидная очистка с получением роданистого аммония (поглотитель полисульфид аммония). Степень очистки 80–85%: (NH4)2Sn + NH3 + HCN = NH4CNS + (NH4)2Sn-1 (NH4)2Sn-1 + S = (NH4)2Sn.
Мышьяково - содовая сероочистка Цех мышьяково-содовой сероочистки состоит из следующих отделений: Улавливания сероводорода и регенерации поглотительного раствора; Плавки и кристаллизации серы; Приготовления содового и мышьякового раствора; 4. Нейтрализации отработанного раствора.
Вакуум - карбонатная сероочистка Цех очистки коксового газа от сероводорода вакуум-карбонатным методом включает: 1. Отделение улавливания и регенерации насыщенного поглотительного раствора 2. Отделение получения серной кислоты методом мокрого катализа. Для улавливания сероводорода из коксового газа используются водные растворы соды (Na2CO3) или поташа (K2CO3).
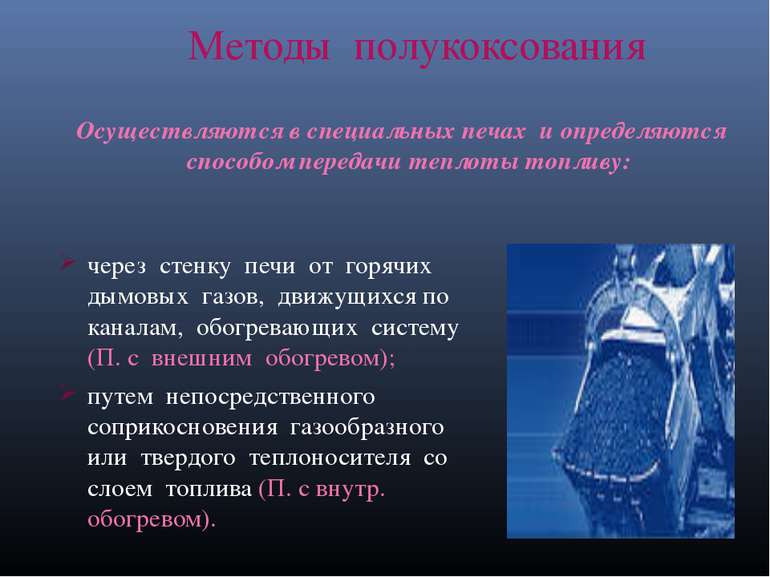
ПОЛУКОКСОВАНИЕ Процесс переработки твердых горючих ископаемых нагреванием без доступа воздуха при 500-600°С (при температуре, примерно вдвое более низкой, чем температура коксования) с целью получения гл. обр. твердого остатка (полукокса), а также летучих продуктов. Сырье - обычно бурые угли и горючие сланцы, реже - каменные угли и торф.
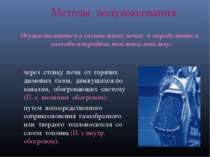
Методы полукоксования через стенку печи от горячих дымовых газов, движущихся по каналам, обогревающих систему (П. с внешним обогревом); путем непосредственного соприкосновения газообразного или твердого теплоносителя со слоем топлива (П. с внутр. обогревом). Осуществляются в специальных печах и определяются способом передачи теплоты топливу:
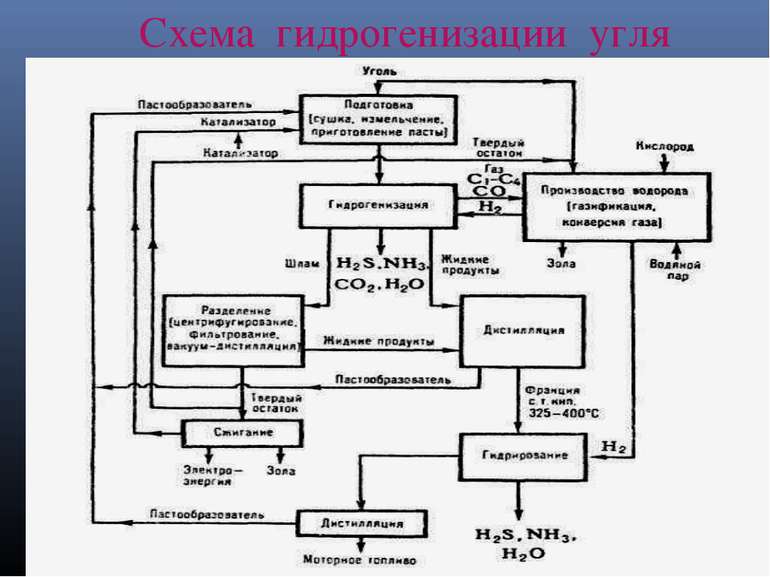
ГИДРОГЕНИЗАЦИЯ Процесс превращения высокомолекулярных веществ органической массы угля (ОМУ) под давлением водорода в жидкие и газообразные продукты при 400-500 °С в присутствии различных веществ - орг. растворителей, катализаторов и т.д. Научные основы этого процесса были разработаны в начале 20 в. В. Н. Ипатьевым, Н. Д. Зелинским, Ф. Бергиусом, Ф. Фишером и др.
Прямая гидрогенизация угля является перспективным методом получения углеводородов. В настоящее время известно несколько освоенных промышленностью способов: Процесс Бергиуса — некаталитическая прямая гидрогенизация; Процесс Шрёдера — гидрогенизация угля в смеси с 1 % масс. молибденового катализатора, в состав реакционной смеси входят: смесь жидких углеводородов — «нафта», ограниченные количества углеводородных газов C3-C4, лёгкого жидкого топлива C5-C10, NH3, значительные количества CO2.
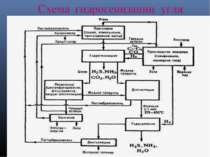
Стадии гидрогенизации угля Подготовка угля; Сушка (влага ~ 1,5%); Нанесение катализатора (из растворов солей в количестве 1-5% от массы угля); Углемасляную пасту в смеси с циркулирующим водородсодержащим газом нагревают в системе теплообмена и трубчатой печи и затем направляют на гидрогенизацию в реактор; Гидрогенизацию осуществляют в трех или четырех последовательно расположенных цилиндрических пустотелых реакторах; Продукты реакции разделяют в сепараторе на парогазовую смесь и тяжелый остаток – шлам.
Из первого потока выделяют: жидкие продукты (масло, воду); газ (к-рый после отделения предельных углеводородов (С1-С4), NH3, H2S, CO2 и СО, Н2О обогащают 95-97%-ным Н2 и возвращают в процесс). Шлам разделяют на: жидкие продукты (после отделения воды подвергают дистилляции на фракцию с т. кип. до 325-400 °С и остаток, который возвращают в процесс для приготовления пасты) ; твердый остаток. Продукты гидрогенизации
ГАЗОФИКАЦИЯ Процесс превращения твердых топлив (углей, торфа, сланцев) в горючий газ, состоящий гл. обр. из СО и Н2, при высокой т-ре в присутствии окислителя (газифицирующего агента). Проводится в газогенераторах (поэтому получаемые газы называются генераторными). Газификацию твердых топлив можно рассматривать как неполное окисление углерода.
Основные реакции Наиболее часто окислителями служат О2 (реакция 1), СО2 (2) и водяной пар (3): Наряду с основными реакциями осуществляются следующие:
"... настанет, вероятно, со временем даже такая эпоха, что угля из земли вынимать не будут, а там в земле его сумеют превращать в горючие газы..." (1888) Д. И. Менделеев : Позднее в 1912 году эту же идею высказал У. Рамзай. В. И. Ленин в статье "Одна из великих побед техники" высоко оценил идею Подземной газификации углей и ее преимущества перед шахтным методом добычи угля. СССР принадлежит приоритет в разработке (с 1930) и внедрении технических решений П. г. у.
Подземная газификация угля Осуществляется под действием высокой температуры (1000-2000 °С) и подаваемого под давлением дутья - различных окислителей (как правило, воздуха, О2 и водяного пара, реже-СО2). Для подвода дутья и отвода газа газификацию проводят в скважинах, расположенных в определенном порядке и образующих так называемый подземный генератор. В нем идут те же хим. реакции, что и в обычных газогенераторах. Газ, производимый путем П. г. у., применяют для энергетических нужд (в осн. как котельное топливо). Себестоимость газа (в пересчете на условное топливо) ниже себестоимости угля, добываемого шахтным способом, и выше себестоимости угля открытой добычи
Источники информации: http://www.chem.asu.ru/org/cpk/spk06.pdf; http://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D1%85%D0%B8%D0%BC%D0%B8%D1%8F; http://www.xumuk.ru/encyklopedia/1029.html; Калея и ц И. В., Химия гидрогенпзационных процессов в переработке топлив, М., 1973; Кричко А. А., Лебедев В. В, Фарберов И. Л., Нетопливное использование углей, М, 1978. А. А. Кричко.; http://www.xumuk.ru/encyklopedia/1029.html; http://www.xumuk.ru/encyklopedia/2/3625.html; Федосеев С. Д., Чернышев А. Б., Полукоксование и газификация твердого топлива, М., 1960; Кузнецов Д. Т , Эпергохимическое использование горючих сланцев, М., 1978; Наумов Л. С , Соболев Л Д , На орбите кокса, М., 1984, с. 16-17; ГлущенкоИМ, Химическая технология горючих ископаемых, К., 1985; Лавров Н. В., Шурыгин А. П., Введение в теорию горения и газификации топлива, М., 1962; Альтшулер В. С, К ли ри ко в Г. В., Медведев В. А., Термодинамика процессов получения газов заданного состава из горючих ископаемых, М., 1969; Эпик И., "Известия АН ЭССР. Сер. Геология", 1982, т. 31, № 2, с. 42-55; его же, "Известия АН ЭССР. Сер. Химия", 1983, т. 32, № 2, с. 81-97; Химические вещества из угля, пер. с нем., под ред. И. В. Калечица, М., 1980. Э.Э. Шпильрайн.
Схожі презентації
Категорії