Презентація на тему:
"Випромінювання та поглинання світла атомами"
Завантажити презентацію
"Випромінювання та поглинання світла атомами"
Завантажити презентаціюПрезентація по слайдам:
Випромінювання та поглинання світла атомами. Атомні і молекулярні спектри. Спектральний аналіз та його застосування Підготувала: ліцеїст 203 н.в. Бондаренко Оксана
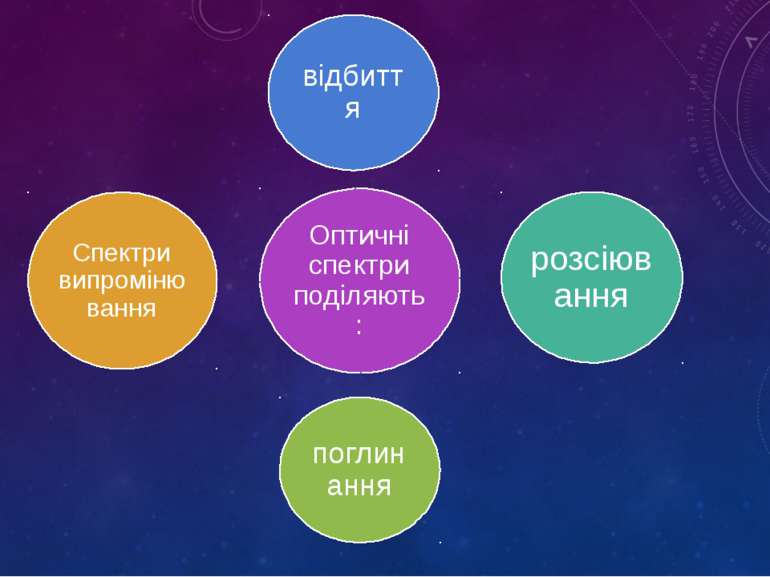
Електромагнітне випромінювання будь-якої природи може характеризуватися спектром коливань, на які можна розкласти його за довжиною хвилі або частотою. Оптичні спектри випромінювання спостерігаються у джерел світла, які випускають фотони внаслідок збудження речовини під впливом зовнішнього чинника.
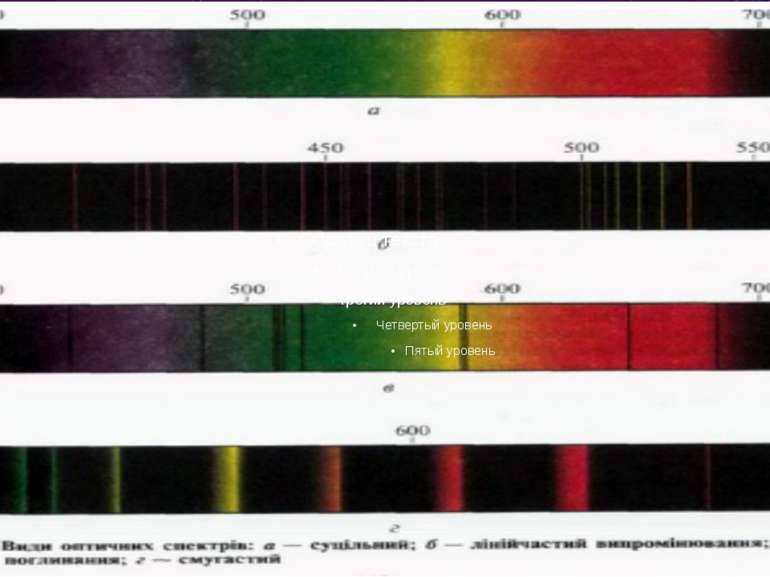
Оптичні спектри спостерігають візуально за допомогою спектральних приладів і фіксують, як правило, фотографічним способом або за допомогою фотоелементів. Спектри можуть бути :
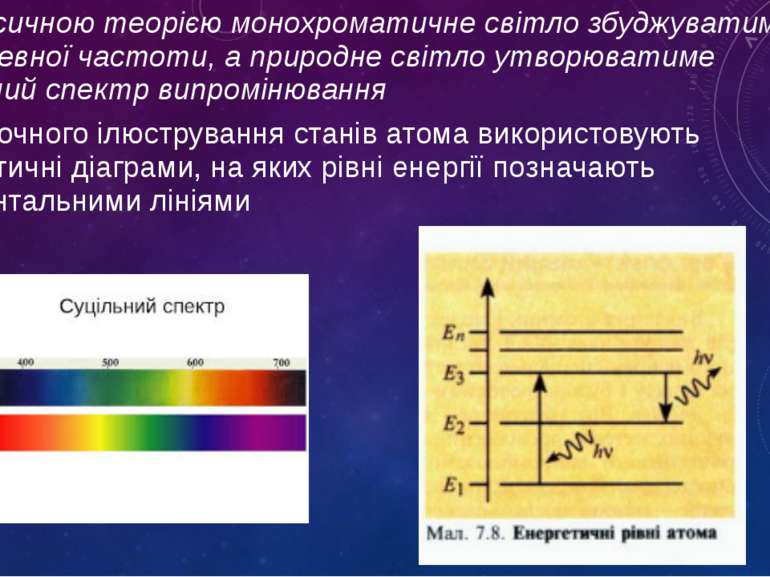
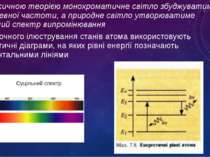
За класичною теорією монохроматичне світло збуджуватиме хвилі певної частоти, а природне світло утворюватиме суцільний спектр випромінювання Для наочного ілюстрування станів атома використовують енергетичні діаграми, на яких рівні енергії позначають горизонтальними лініями
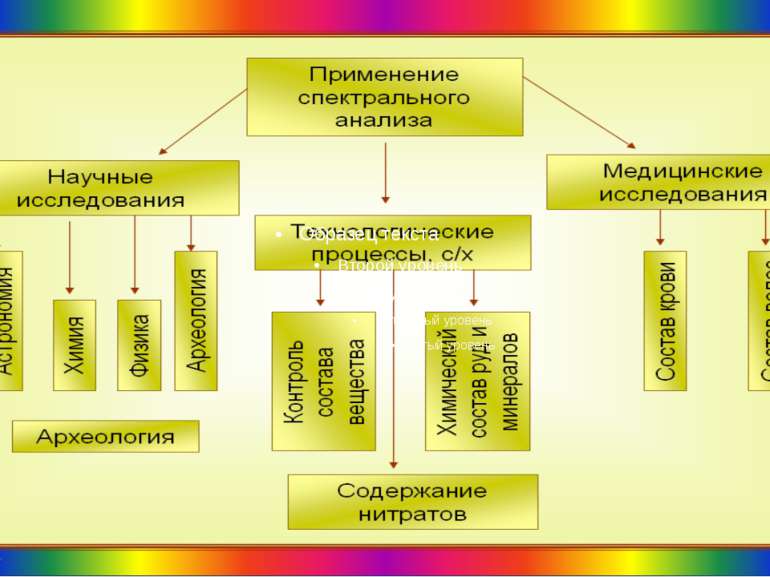
Спектральний аналіз Вивчення атомних і молекулярних спектрів випромінювання і поглинання покладено в основу спеціального методу дослідження складу і будови речовини — спектрального аналізу. Він грунтується на кількісних і якісних методах дослідження спектрів електромагнітного випромінювання речовин, які спостерігають за допомогою спеціальних приладів. Принцип дії цих приладів грунтується на їх здатності виокремлювати в просторі і часі з усього світлового потоку певні ділянки випромінювання. їх можна фіксувати фотографічним способом або вимірювати різні їхні характеристики — зміну світлового потоку, довжину хвилі спектральної лінії тощо. Спектральний аналіз ґрунтується на явищі дис персії світла.
Історія Ідентифікація хімічних елементів за оптичними спектрами атомів була запропонована у 1859 році Г. Кірхгофом та Бунзеном. За допомогою спектрального аналізу, гелій (He) був відкритий на Сонці раніше ніж на Землі. Але ще у 1854 році доктор Девід Альтер (англ. David Alter), науковець з міста Фріпорт, штату Пенсильванія (США) надрукував наукову працю, що описувала спектральні властивості 12 металів .
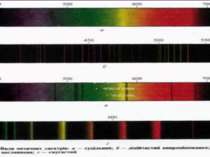
Кожен хімічний елемент має власний набір спектральнихліній, притаманний лише йому одному. Для одержання спектра випромінювання атоми речовини слід перевести у збуджений стан, наприклад нагріти тіло до високої температури. За високих температур атоми переходять у збуджений стан Е2, E3, Е4, Е5, в якому можуть перебувати недовго
Спектральний аналіз виконується за допомогою спектрометра Спектро метр - спектральний прилад зі сканувальним пристроєм, який за допомогою фотоелектричних приймачів дає змогу кількісно оцінювати розподіл енергії у спектрі. Термін застосовується до приладів, що працюють у широкому діапазоні хвиль: від гамма- до інфрачервоного випромінювання.
Схожі презентації
Категорії