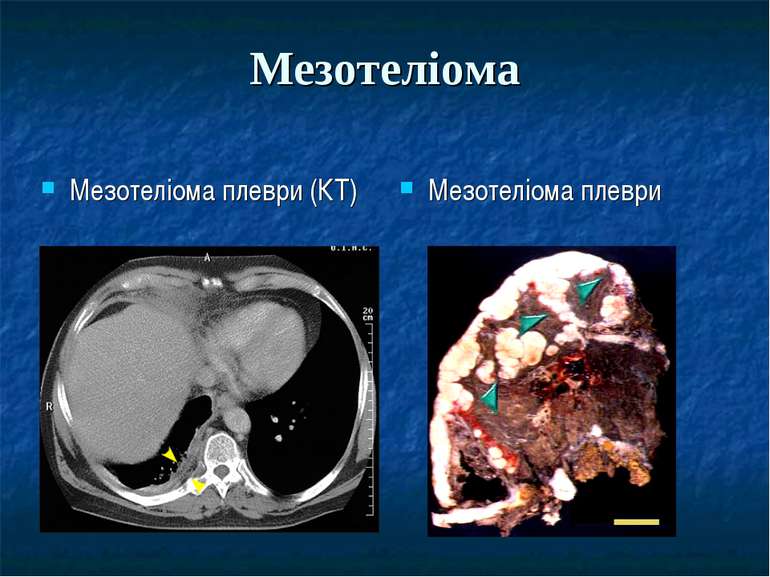
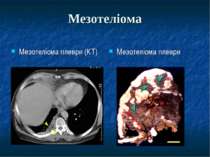
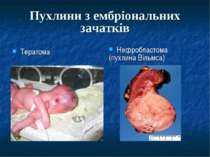
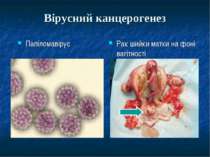
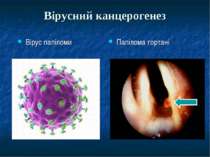
Презентація на тему:
онкологія
Завантажити презентацію
онкологія
Завантажити презентаціюПрезентація по слайдам:
Онкозахворювання, епідеміологія, основні причини раку. Онкозахворюваність, структура, облік і динаміка. Класифікація онкозахворювань, система ТNМ. Організація і задачі онкослужби. Протиракова боротьба, диспансеризація онкохворих. Профілактика онкозахворювань Крижанівська А.Є. Івано-Франківський національний медичний університет Кафедра онкології
Онкологія (від грецького oncos - пухлина, lоgos - наука) - наука, яка вивчає причини виникнення, механізм розвитку та клінічні прояви пухлини, а також методи їх діагностики, лікування та профілактики
Історія онкології – стародавній Єгипет В єгипетських папірусах за 3000 років до н.е згадується про пухлинні захворювання грудей.
Історія онкології - Гален виникнення терміну «рак» «Ми часто бачили на грудях жінок пухлину схожу на рака (cancer), так як і в рака у цієї хвороби є жили які виходять з неї в інші частини тіла і нагадують клешні…» Гален Пергамський (II століття до н.е.).
Історія онкології - Гіпократ У випадках скритого раку краще не застосовувати ніякого лікування, оскільки ліковані хворі швидко помирають, а без лікування можуть прожити довго. Трактат «Про карциноз», афоризм 38 (250 років до н.е.)
Історія онкології - Геродот Описуючи рак молочної залози у Атоси – жінки Дарія, Геродот дорікав їй за легковажне відношення до захворювання. З її сторони це було цілком зрозуміло – в ті часи загальноприйнятним способом лікування пухлин було «випікання» розпеченим залізом… (230 років до н.е.)
Скам’янілі залишки нижньої щелепи гомініда з ознаками остеосаркоми знайдені у Східній Африці (1 млн.років тому). ХIV століття - саксонський хірург Джон з Ардену описав рак прямої кишки. 1700р. – Рамацоні встановив високу захворюваність монахинь на рак молочної залози. 1700р. Гендрон опублікував «Гіпотези про причини» - лікувати можна тільки локальні пухлини. Ле-Дран (1685-1770) – висловив припущення, що рак виникає як локальна пухлина і поширюється з «лімфою». Рекам’є (1774-1852) – описав процес метастазування. 1740р. – Персіваль Пот встановив причину раку шкіри у сажотрусів, Датська гільдія сажотрусів наказала миття тіла після роботи (перший приклад успішної профілактики раку).
Історія онкології – лікування раку Протягом багатовікової історії людства епізодично застосовувались методи видалення чи «випікання» пухлин зовнішніх локалізацій. Перші успішні операції при раку сигмовидної кишки (Реубард,1833р.), шлунка (Більрот,1874р., Пеан, 1879р., Шлатер, 1898р.), молочної залози (Холстед, 1889р.), нирки (Орловський, 1884р.). Вільям Конрад Рентген 8.10.1895р. відкрив Х-промені. П’єр і Марія Кюрі 1.03.1896р. відкрили радій. 3 грудня 1943 р. після бомбардування і вибуху в порту Барі 100 т. гірчичного газу, американський лікар Джон Александер звернув увагу на виражені зміни під впливом іприту в кістковому мозку і лімфовузлах – це послужило поштовхом до виникнення хіміотерапії раку. Розробка ефективної вакцини для профілактики раку шийки матки – 2005р.
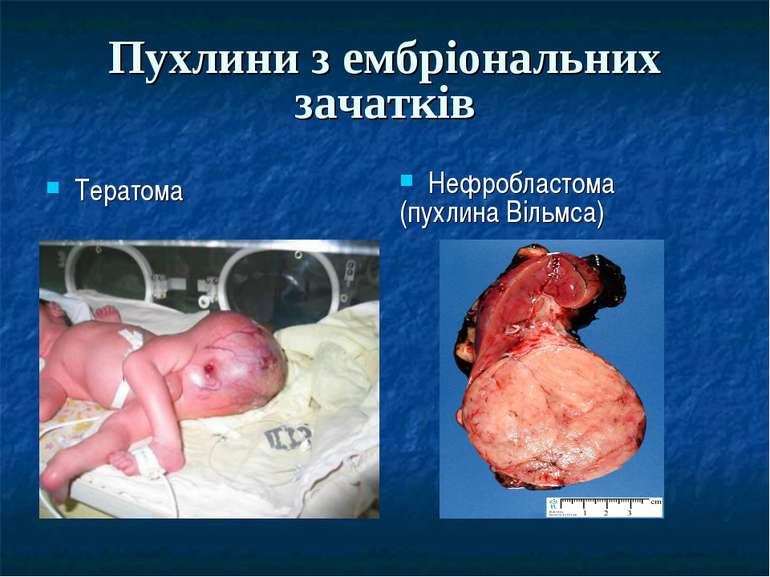
Теорії канцерогенезу. Конгейм (Cohnheim) Юліус Фрідріх - німецький патолог (1839-1884). Основна робота Конгейма — курс загальної патології, в якому викладено вчення про походження пухлин (так звана «теорія ембріональних зачатків Конгейма»). Згідно якої, пухлини розвиваються з ембріональних зачатків, які залишились невикористаними в періоді виникнення і росту зародка; з часом при послабленні життєдіяльності навколишніх тканин ці клітини, на думку Конгейма, починають посилено розмножуватися.
Теорії канцерогенезу. Рудольф Вірхов, німецький патологоанатом (1821-1902) – теорія хронічного запалення. В кінці 19 століття Рудольф Вірхов висунув теорію “хронічного запалення”, згідно якої тривале подразнення і хронічна травма ведуть до виникнення пухлин.
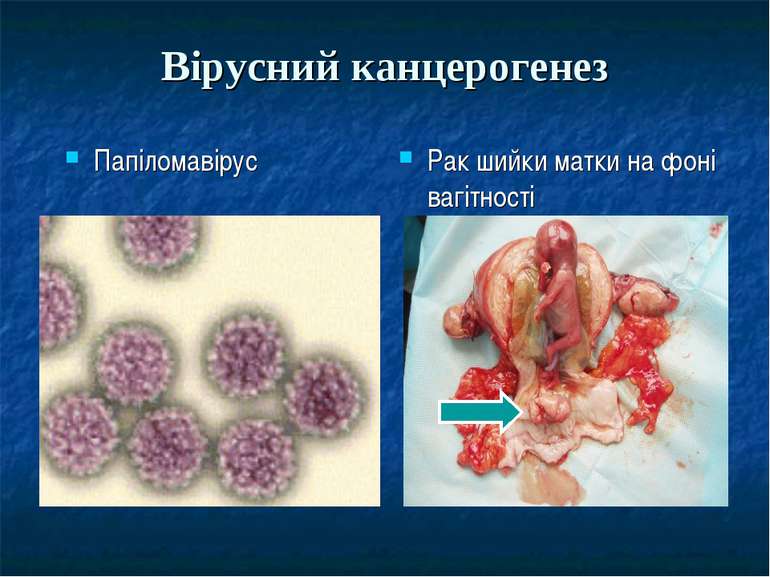
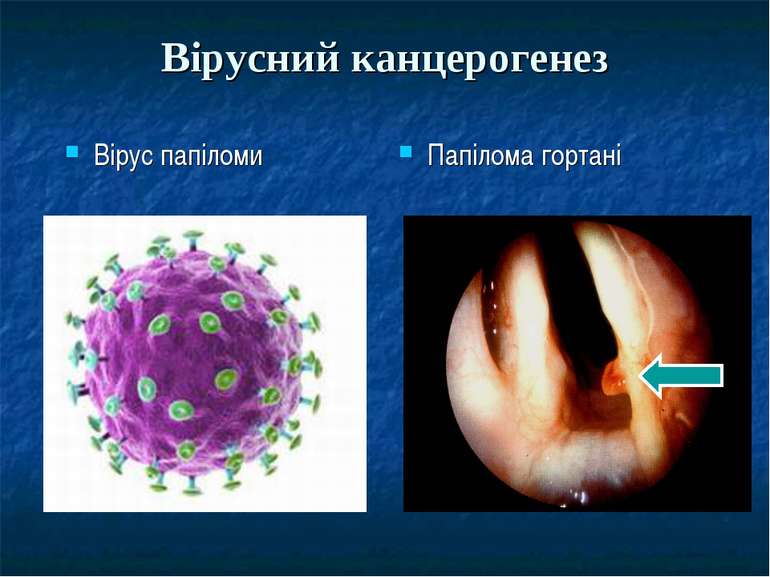
Теорії канцерогенезу. Зільбер Лев Олександрович (1894-1966р.). В 1946 р. Л.О.Зільбер розробив вірусну, а пізніше вірусно-генетичну теорію раку. Суть її полягає в тому, що інтеграція онкогенного вірусу в геном клітини, призводить до її пухлинної трансформації.
Пухлини Доброякісні зрілі експансивний ріст тканинний атипізм не метастазують Злоякісні незрілі інфільтративний ріст клітинний атипізм метастазують
Біологічні особливості пухлинної клітини Тканинний атипізм - зміна співвідношення між паренхімою і стромою, частіше з перевагою паренхіми. Клітинний атипізм проявляється клітинним і ядерним поліморфізмом: зміна форми, розмірів, будови, забарвлення, кількості, розмірів, форми хромосом (Ph-хромосоми при СМL). Морфологічна атипія - порушення органотипічного, гістотипічного, цитотипічного диференціювання. У доброякісних пухлинах - порушення органотипічного і гістотипічного диференціювання. У злоякісних - характерно в першу чергу порушення цитотипічного диференціювання.
Біологічні особливості пухлинної клітини Атипізм розмноження – безконтрольне розмноження (культура клітин асцитичної карциноми Ерліха мишей існує з 1905р., культура клітин HELA з 1951р. ). Атипізм енергетичний і метаболічний: - інтенсивний синтез онкобілків, які забезпечують основні ознаки пухлини (безконтрольне розмноження, безсмертя, здатність до інвазії та ін.); - зменшення синтезу білків-супресорів синтезу ДНК (гістонів); - синтез ембріональних білків (наприклад АФП); - енергетичні зміни – збільшення частки гліколізу; - посилене захоплення та використання («пожирання») глюкози і амінокислот.
Безсмертя пухлинних клітин 1 В 1951 році в госпіталі Університету Джона Хопкінса (США) була виконана біопсія з цервікального каналу у пацієнтки з пухлиною шийки матки. Пацієнтці, Генрієті Лакс з Балтимора, було тоді тридцять один рік, вона померла через вісім місяців. Клітини її пухлини живуть до теперішнього часу у вигляді культури пухлинної тканини HELA.
Біологічні особливості пухлинних клітин Атипізм фізико-хімічний: збільшення вмісту води і калію (стимуляція росту і розмноження), зменшення вмісту кальцію і магнію (зменшення міжклітинної адгезії, розвиток здатності до інвазії і метастазування); збільшення від’ємного заряду клітини і електропровідності. Функціональний атипізм - втрата, посилення, спотворення функцій, невідповідність функціонування пухлинної тканини регуляторним впливам. Спотворення проявляється в придбанні пухлинною тканиною не характерних для неї функцій (синтез кальцитоніну раковими клітинами молочної залози, синтез клітинами пухлини легень- гормонів гіпофізу АКТГ чи АДГ) - ектопічний ендокринний синдром.
Метастазування – найбільш важлива і небезпечна ознака пухлинної прогресії Метастазування – утворення вторинних пухлинних вогнищ завдяки придбанні пухлинними клітинами здатності до інвазії в навколишні тканини, проникання в кровоносні і лімфатичні судини, виживання і розмноження в не властивому мікрооточенні. Лімфогенні метастази – метастази пухлини в регіонарних лімфовузлах. Гематогенні метастази – вторинні пухлинні вогнища в інших органах, внаслідок гематогенного поширення пухлинних клітин (емболів). Імплантаційні метастази виникають внаслідок поширення пухлинних клітин по поверхні.
Злоякісні новоутворення захворювання, що виникають в результаті патологічного розростання клітин, які характеризуються функціональною, метаболічною і структурною атипією і схильність до безконтрольного розмноження (автономність, нерегульованість, втрата функції контактного гальмування, невпорядковане розміщення, схильність до пенетрації і метастазування, примітивний метаболізм, морфологічна і генетична атипія).
Злоякісні новоутворення одна з найважливіших медико-біологічних та соціально-економічних проблем охорони здоров’я; стабільно зростають; визначають рівень здоров’я нації; ризик захворіти збільшується через несприятливу екологічну ситуацію та значне старіння населення; у 22-26 % випадків - зумовлюють інвалідизацію
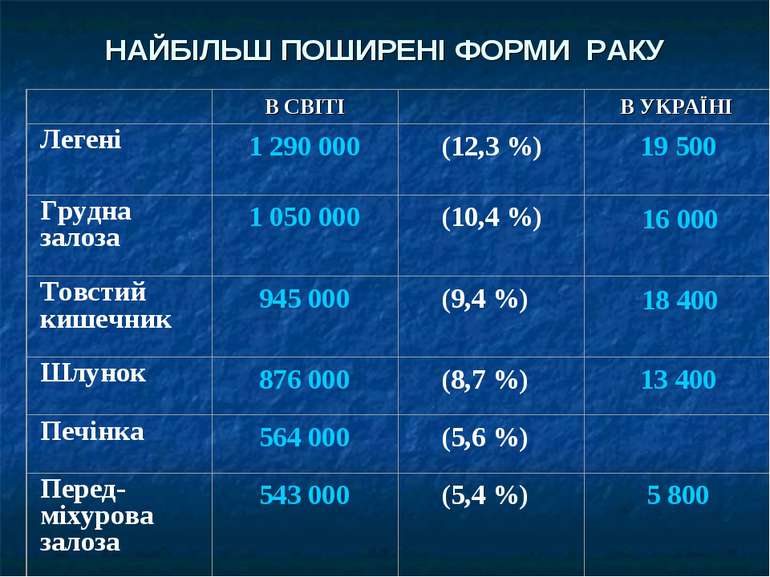
Захворюваність і смертність Захворюваність – кількість захворівших злоякісними новоутвореннями на 100 000 населення в рік. Смертність - кількість померших від раку на 100 000 населення в рік. Кожного року в світі хворіє на рак більше 10 млн. людей і приблизно 8 млн. помирають від нього. Критерієм успішного лікування раку є 5 – річна виживаність – кількість хворих (%), які пережили 5-ти річний термін після встановлення діагнозу.
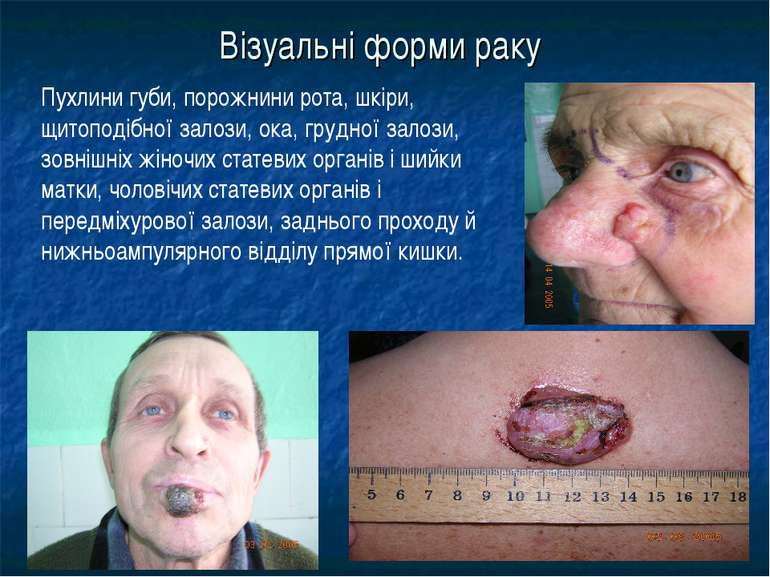
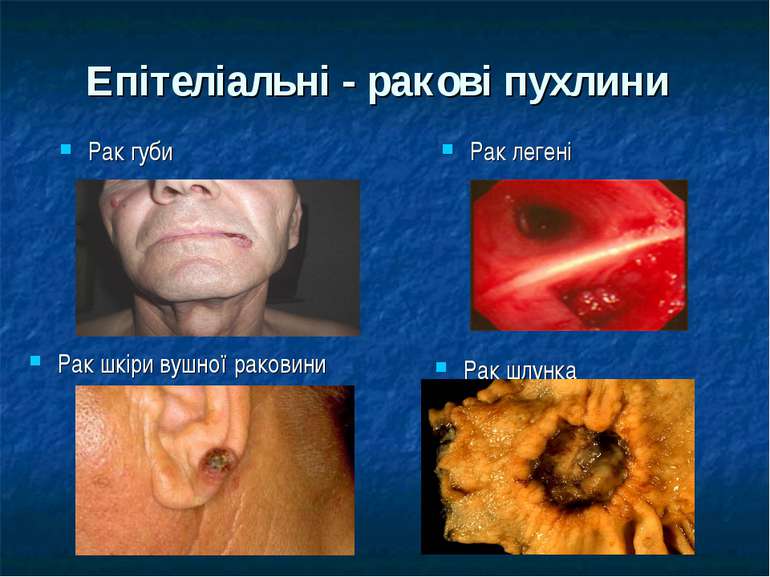
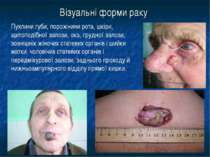
Візуальні форми раку Пухлини губи, порожнини рота, шкіри, щитоподібної залози, ока, грудної залози, зовнішніх жіночих статевих органів і шийки матки, чоловічих статевих органів і передміхурової залози, заднього проходу й нижньоампулярного відділу прямої кишки.
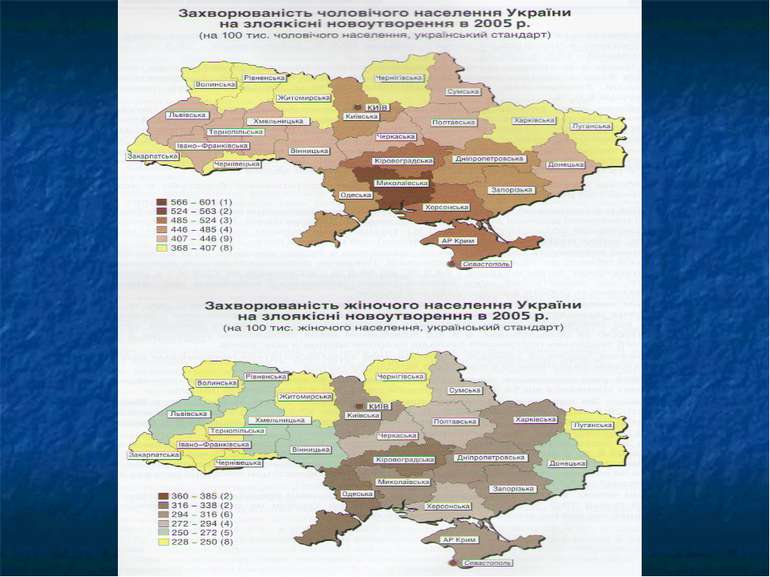
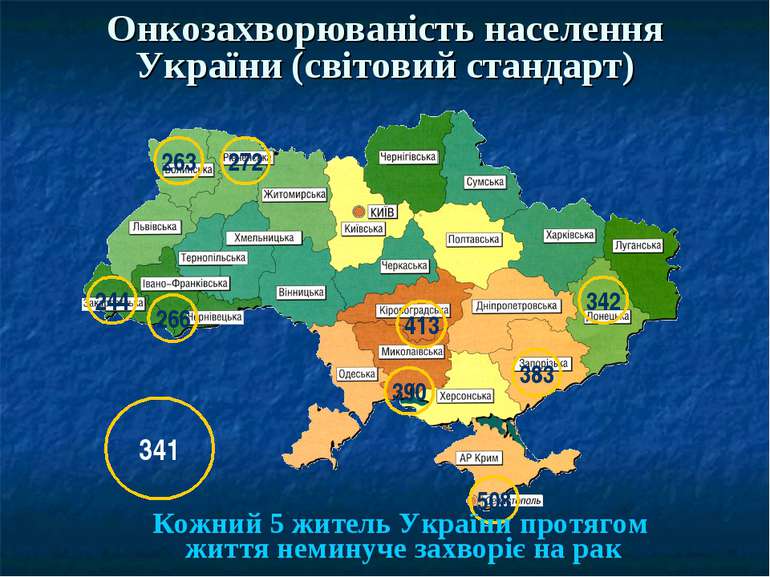
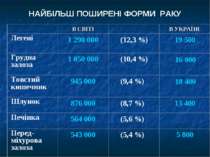
Онкозахворюваність населення України (світовий стандарт) 244 266 263 272 390 413 383 508 342 341 Кожний 5 житель України протягом життя неминуче захворіє на рак
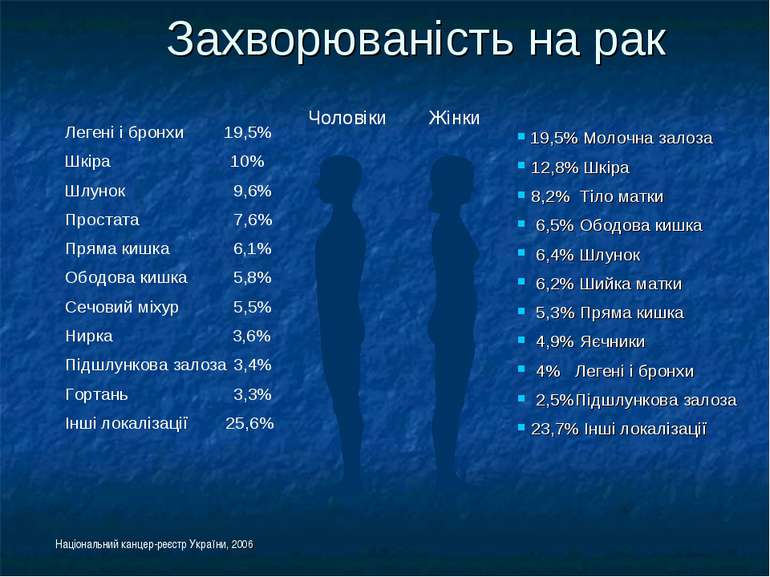
Захворюваність на рак Національний канцер-реєстр України, 2006 Чоловіки Жінки 19,5% Молочна залоза 12,8% Шкіра 8,2% Тіло матки 6,5% Ободова кишка 6,4% Шлунок 6,2% Шийка матки 5,3% Пряма кишка 4,9% Яєчники 4% Легені і бронхи 2,5% Підшлункова залоза 23,7% Інші локалізації Легені і бронхи 19,5% Шкіра 10% Шлунок 9,6% Простата 7,6% Пряма кишка 6,1% Ободова кишка 5,8% Сечовий міхур 5,5% Нирка 3,6% Підшлункова залоза 3,4% Гортань 3,3% Інші локалізації 25,6%
Смертність від раку Національний канцер-реєстр України, 2006 Чоловіки Жінки 20,3% Молочна залоза 10,2% Шлунок 8% Ободова кишка 6,8% Пряма кишка 6,2% Яєчники 5,9% Легені і бронхи 5,7% Шийка матки 5,4% Тіло матки 4,4% Підшлункова залоза 2,8% Лейкемії 24,3% Інші локалізації Легені і бронхи 26% Шлунок 12,1% Простата 6,3% Пряма кишка 6,2% Ободова кишка 5,7% Підшлункова залоза 4,5% Сечовий міхур 4,3% Гортань 3,3% Нирка 3,2% Порожнина рота 3% Інші локалізації 25,4%
Медична документація на онкологічних хворих “Повідомлення про хворого з вперше в житті встановленим діагнозом раку або іншого злоякісного новоутворення” – форма №090/о, “Протокол на випадок виявлення у хворого занедбаної форми злоякісного новоутворення” – форма №027-2/о заповнює лікар, який виявив захворювання і у триденний термін відправляє в онкодиспансер
Складові частини онкологічного діагнозу Назва пухлини у відповідності з міжнародною морфологічною класифікацією злоякісних новоутворень. Локалізація органа або анатомічної ділянки, де є пухлина. Стадія за системою ТNM. Клінічна група – як умовне поняття, яке визначає тактику лікаря по відношенню до діагностики, лікування та диспансеризації хворого на рак.
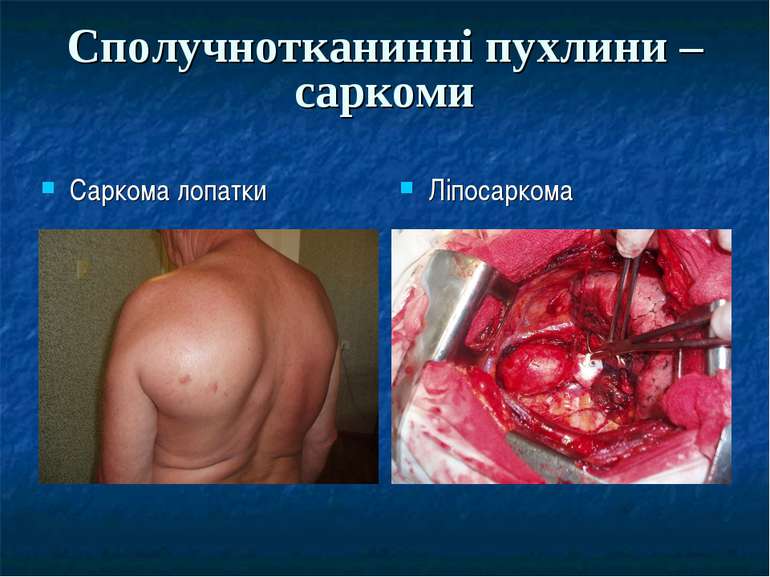
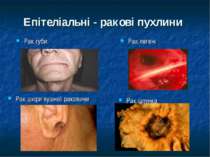
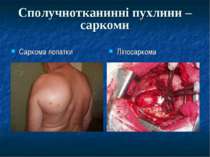
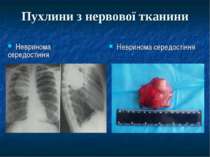
Морфологічна класифікація злоякісних новоутворів Рак – епітеліальні пухлини (з плоского епітелію – плоскоклітинний рак, зі залозистого епітелію – аденокарцинома) Саркома – пухлина зі сполучної тканини (фібро-, хондро-, остео-, рабдоміо- і лейоміосаркоми, ліпосаркома) Гемобластози – новоутвори системи крові системні – лейкози пухлини (лімфогрануломатоз та негоджкінські лімфоми) Пухлини з APUD–системи – апудоми (феохромоцитома, меланома, дрібноклітинний рак легень) Рідкісні форми - хоріонепітеліома, тератобластома, семінома
TNM – міжнародна класифікація злоякісних пухлин T1 - пухлина до 2 см або займає один шар стінки органа Т2 - пухлина до 5 см або інфільтрує декілька шарів стінки органа Т3 – пухлина більша 5 см або проростає всі шари стінки органа чи навколишню клітковину Т4 – пухлина поширюється на сусідні органи N0 - метастази в лімфовузлах відсутні N1 - ураження реґіонарних лімфатичних вузлів N2 - передбачено для РШ, РТК, N3 – визначається при РМЗ, РЛ, РН, РСМ, Р яєчка та пухлинах голови і шиї М0 - віддалені метастази відсутні М1 - наявні віддалені метастази
Клінічні групи Iа - охоплює усіх хворих, у яких лікар запідозрив рак. Необхідно у 10-денний термін підтвердити або заперечити діагноз, Iб - усі хворі з передпухлинною патологією. II - хворих на злоякісні новоутвори, які вимагають спеціального лікування з надією на одужання - (IIа) або ремісії (II). III – практично здорові люди, які закінчили радикальне лікування. IV - хворі у IV стадії захворювання, більшості із них проводиться тільки симптоматичне лікування (у т.ч. - хірургічне – при ускладненнях, променеве – для зняття больового синдрому, хіміотерапевтичне для покращення якості та тривалості життя).
Основні причини виникнення злоякісних пухлин Куріння – 30 % Особливості харчування – 35 % Інфекції – 10 % Професійні фактори – 4-5 % Іонізуюче випромінювання – 4-5 % Алкоголь – 2-3 % Ультрафіолетове випроміннювання – 2-3 % Забруднення атмосферного повітря – 1-2 % Репродуктивні фактори – 4-5 % Низька фізична активність – 4-5 %
Канцерогенез це багатоступеневий процес накопичення мутацій та інших генетичних змін клітини, порушення регуляції розмноження і міграції клітин, зниження чутливості клітин до зовнішніх регулючих сигналів, блокування механізмів диференціювання і апоптозу, розвитку і наростання процесів пухлинної прогресії.
Причини виникнення раку Мутація нормального гена призводить до виникнення раку. Мутований ген, що спричиняє рак називається онкогеном. Необхідно декілька мутацій, щоб почався ріст пухлини Старі клітини, або ті, що не функціонують, відмирають і їх місце займають нові. Однак, ракові клітини не відмирають, продовжують швидко ділитися і продукують мільйони нових ракових клітин.
Генетичні механізми канцерогенезу Онкогени – клітинні (внутрішні) чи вірусні (зовнішні) гени, експресія яких збільшує ймовірність виникнення чи прогресування злоякісної пухлини. Протоонкогени – нормальні клітинні гени посилення чи зміна функції яких перетворює їх в онкогени. Пухлинні супресори – клітинні гени, які пригнічують пухлинний ріст (їх інактивація веде до прогресії пухлини). Мутаторні гени – гени, які мають властивість збільшувати інтенсивність мутацій чи інших генетичних змін, які призводять до малігнізації.
Канцерогени Іонізуюча радіація – рентгенівське і ультрафіолетове опромінення Хімічні – смола зі сигарет Вірусна інфекція – папіломовірусна інфекція, яка призводить до раку шийки матки Генетична схильність – у деяких родинах існує вища ймовірність виникнення раку
Хімічні речовини з доказаною канцерогенністю 4-амінобіфеніл; азатіоприн, азбест, афлатоксин, бензидин, бензол, берилій, кадмій, миш’як, хром, нікель та їх сполуки, хлорметиловий ефір, хлорнафазін, 1,4-бутандіол диметилсульфонат, вінілхлорид, гірчичний газ, кристалічний кремній, 2-нафтиламін, радон, випари сірчаної кислоти, тальк, 2,3,7,8 – тетрахлордибензопара-діоксин, оксид етилену. З 4 мільйонів відомих науці хімічних сполук на канцерогенну активність досліджено близько тисячі (0,025%).
Суміші з доказаною канцерогенністю Куріння Рак порожнини рота, губ, глотки, стравоходу, шлунка, печінки, підшлункової залози, гортані, легені, нирки, сечового міхура, шийки матки, мієлоїдний лейкоз. Табак не для куріння Рак породнини рота, носа, носових пазух Пасивне куріння Рак легені Алкоголь Рак порожнини рота, глотки, гортані, стравоходу, шлунка, печінки, підшлункової залози. Кам’яновугільний пек, смола, дьоготь, сажа Рак шкіри, калитки, легені, сечового міхура Мінеральні і сланцеві масла Рак шкіри, калитки, легені Солена риба китай-ського приготування Рак носоглотки, стравоходу, шлунка Деревний пил Рак порожнини і пазух носа
Промислові процеси з доказаною канцерогенністю Алюмінієва промисловість Рак легені, сечового міхура Виробництво аураміну і фуксину Рак сечового міхура Газифікація і коксування вугілля Рак легені, шкіри, сечового міхура, калитки, нирки Видобування гематиту Рак легені Виробництво ізопропілового спирту Рак пазух носа, легені, гортані Літійна промисловість Рак легені Мебельна промисловість Рак пазух носа Малярні роботи Рак легені, сечового міхура Взуттєва промисловість Лейкоз, лімфома Резинова промисловість Рак легені, сечового міхура, шлунка, товстої кишки, простати, шкіри, гемобластози
Фізичні канцерогени Ультрафіолетові промені сонячного спектру - максимальний біологічний ефект спостерігається при довжині хвилі 280-320 нм. (В 2009р. МАІР офіційно заявило про те, що штучний загар в солярії підвищує ризик розвитку меланоми на 75%). Іонізуюче випромінювання: електромагнітне (фотонне) - рентгенівське і гамма-випромінювання, корпускулярне – альфа і бета-промені. Повторні опіки, механічна травма.
Біологічні канцерогени Віруси гепатиту В і С Гепатоцелюлярний рак Вірус Т-клітинного лейкозу дорослих Т-клітинний лейкоз дорослих Вірус папіломи людини 16 і 18 типів Рак шийки матки Вірус Епштейна - Барра Лімфома Беркіта, лімфогранулематоз, рак носоглотки, рак шлунка Вірус імунодефіциту Саркома Капоші, лімфоми Канцерогенні бактерії і паразити Helicobacter pylori Рак шлунка Schistosoma haemotobium Рак сечового міхура Opistorchis viverrini Холангіоцелюлярний рак
Теорія вірусного канцерогенезу Існує припущення, що багато пухлин є наслідком вірусного канцерогенезу, але доказати це важко, так як рак відноситься до інтеграційних патологічних процесів, при якому онкоген спочатку вбудований в геном клітини і його ідентифікація неможлива чи затруднена, таким чином, при кожному поділі появляються нові клітини, які вже мають патологічні гени.
Стадії канцерогенезу 1. Трансформації. Спостерігається перетворення протоонкогенів в результаті включення промотора (ампліфікації, транслокації, інсерції, трансдукції, точкової мутації) в активні клітинні онкогени. На ранній стадії виникає іморталізація- клітинне безсмертя. Проходить експресія активних клітинних онкогенів, синтез онкобілків, які є ростовими факторами чи рецепторами факторів росту. Це призводить до безперервного процесу проліферації і трансформована клітина стає джерелом пухлини. На завершальній стадії виникає здатність клітин до трансплантації. 2. Проліферація (активації, промоції) чи розмноження. Геном клітини змінений в напрямку безконтрольної гіперплазії, що призводить до формування первинного пухлинного вузла, потім утворення пухлини. 3. Прогресія пухлини. Наростання ознак злоякісності пухлини виражено в більшій степені, ніж її кількісний ріст. До цього призводить нестабільність геному ракової клітини і формування більш злоякісних клонів в результаті екзо-впливів і ендореакцій.
Основні періоди виникнення пухлини Процес виникнення пухлини триває декілька років (в залежності від виду пухлини) і включає три основні етапи: фаза ініціації - поява, під впливом канцерогенів, латентної пухлинної клітини, яка має генетичні зміни, які закріплені – структурні і функціональні порушення, але не здатність до поділу; фаза промоції - під впливом повторної дії канцерогенів чи промоторів канцерогенезу клітина набуває основні риси злоякісної пухлини і властивість до безмежного поділу – початок пухлинного росту; пухлинна прогресія – подальше спрощення структури і втрата функції пухлинними клітинами, а набування здатності до інвазії в навколишні тканини і метастазування.
Основні періоди розвитку пухлини Доклінічний період – час безсимптомного розвитку пухлини від виникнення пухлинної клітини до появи перших симптомів захворювання: - протягом декількох років, через 20 періодів подвоєння пухлинної маси пухлина досягає об’єму 1 куб.мм (1 мільйон пухлинних клітин) і може бути виявлена тільки випадково; - ще через 10 подвоєнь пухлинної маси об’єм пухлини досягає 1 куб.см (1 мільярд пухлинних клітин) – пухлина може бути діагностована при ціленаправленому дослідженні.
Основні періоди розвитку пухлини Клінічний період – розвиток захворювання на протязі 2-4 років, з моменту появи перших симптомів до смерті хворого (за час від 30-го до 40-го періодів подвоєння маса пухлини досягає 1-1,5 кг). Клінічний період супроводжується розвитком симптомів спочатку обумовлених власне пухлиною, потім пов’язані з порушенням функції органу і появою віддалених метастазів.
Ранній рак Ранній рак – початкова пухлина, яка розвивається в межах слизової і, як - правило, не здатна до метастазування. Радикальне хірургічне лікування багатьох пухлин в стадії «раннього раку» призводить до повного виліковування. В теперішній час не має специфічних маркерів і методів лабораторної діагностики раннього раку. Діагноз «ранній рак» може бути поставлений тільки на основі морфологічного дослідження.
Спадково-зумовлені пухлини Спадкові форми злоякісних пухлин складають близько 7% і поділяються на три групи: Перша група - успадкування гену, який викликає певну форму раку (ретинобластома, пухлина Вільмса). Друга група - успадкування гену, який збільшує ризик розвитку раку певної локалізації (рак молочної залози, пігментна ксеродерма). Третя група – полігенне успадкування: пухлина виникає при поєднанні у хворого декількох спадкових ознак, які пов’язані з порушенням імунітету.
Фактори ризику виникнення раку Паління тютюну Харчування Ожиріння Спеціальність Вид занять Генетична схильність Інфекції Репродуктивність Соціально-економічний статус Забруднення середовища Ультрафіолет Радіація Вживання медикаментів Електромагнітне поле
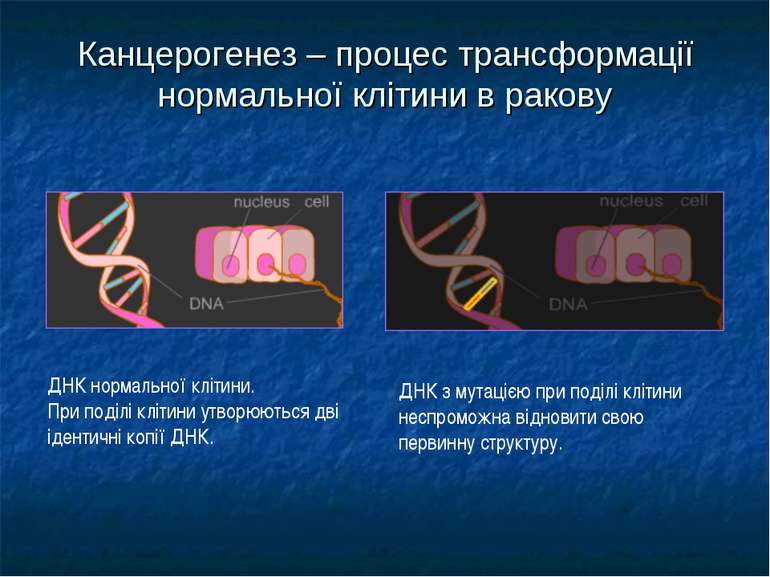
Канцерогенез – процес трансформації нормальної клітини в ракову ДНК нормальної клітини. При поділі клітини утворюються дві ідентичні копії ДНК. ДНК з мутацією при поділі клітини неспроможна відновити свою первинну структуру.
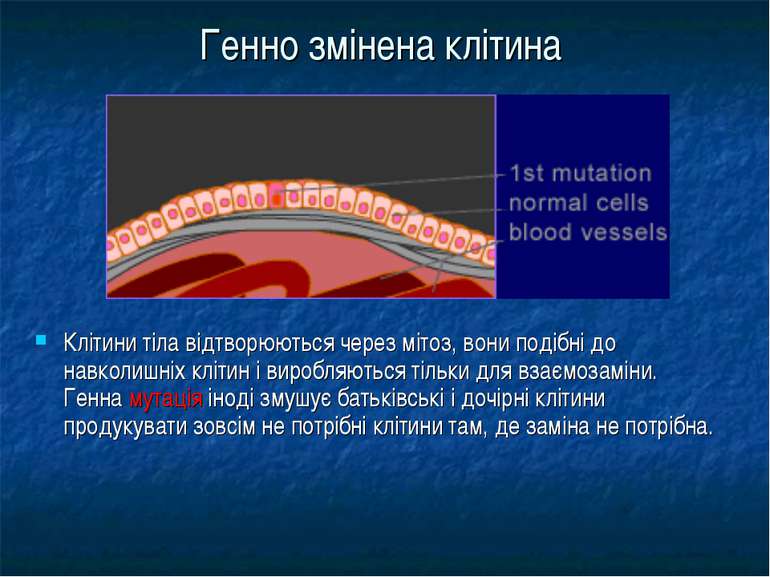
Генно змінена клітина Клітини тіла відтворюються через мітоз, вони подібні до навколишніх клітин і виробляються тільки для взаємозаміни. Генна мутація іноді змушує батьківські і дочірні клітини продукувати зовсім не потрібні клітини там, де заміна не потрібна.
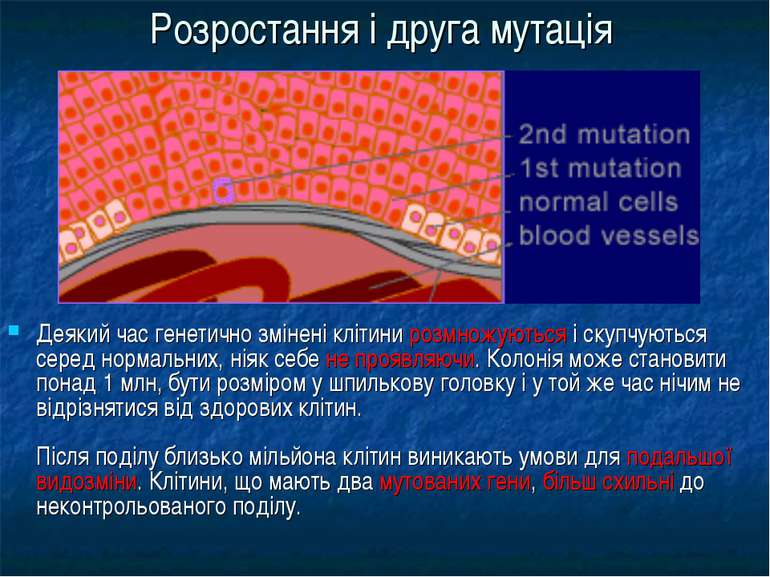
Розростання і друга мутація Деякий час генетично змінені клітини розмножуються і скупчуються серед нормальних, ніяк себе не проявляючи. Колонія може становити понад 1 млн, бути розміром у шпилькову головку і у той же час нічим не відрізнятися від здорових клітин. Після поділу близько мільйона клітин виникають умови для подальшої видозміни. Клітини, що мають два мутованих гени, більш схильні до неконтрольованого поділу.
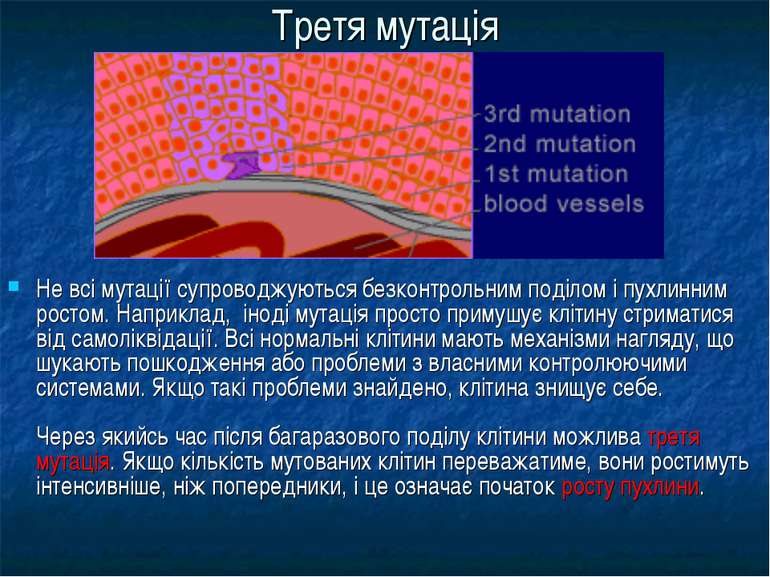
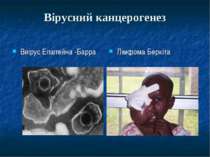
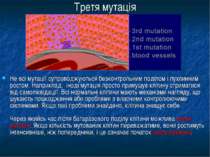
Третя мутація Не всі мутації супроводжуються безконтрольним поділом і пухлинним ростом. Наприклад, іноді мутація просто примушує клітину стриматися від самоліквідації. Всі нормальні клітини мають механізми нагляду, що шукають пошкодження або проблеми з власними контролюючими системами. Якщо такі проблеми знайдено, клітина знищує себе. Через якийсь час після багаразового поділу клітини можлива третя мутація. Якщо кількість мутованих клітин переважатиме, вони ростимуть інтенсивніше, ніж попередники, і це означає початок росту пухлини.
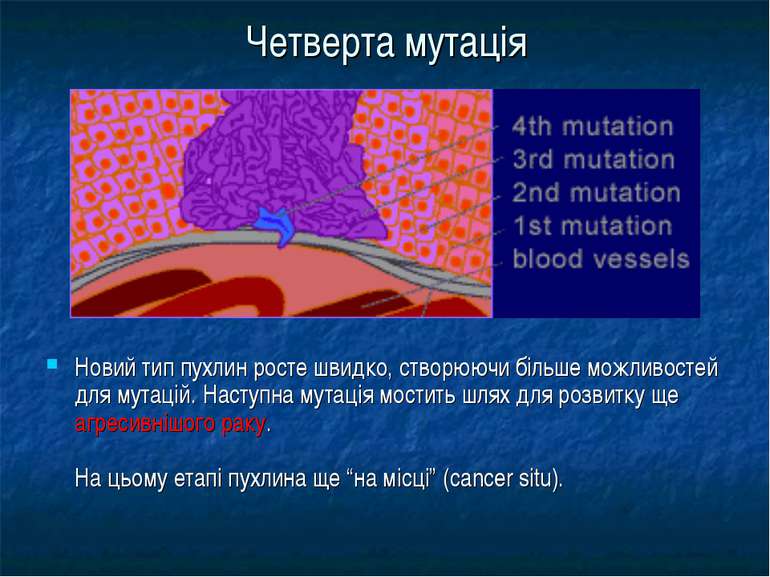
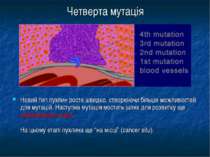
Четверта мутація Новий тип пухлин росте швидко, створюючи більше можливостей для мутацій. Наступна мутація мостить шлях для розвитку ще агресивнішого раку. На цьому етапі пухлина ще “на місці” (cancer situ).
“Прорив” крізь мембрану Нові, агресивніші клітини, створені наступною мутацією, можуть пробити собі шлях через епітеліальну тканину базальної мембрани, яка є протеїновою сіткою і служить природнім бар’єром. Інвазивні клітини більше не можуть залишатися “на місці”. На цьому етапі рак ще замалий, щоб його можна було виявити.
Ангіогенез Часто на ранніх стадіях розвитку пухлини, можливо в часі проростання її через базальну мембрану, розпочинається ангіогенез – “народженння” нових кровоносних судин від уже існуючих. Без постачання крові і поживних речовин пухлина була б не в змозі продовжувати ріст. Нове кровопостачання значно прискорює ріст пухлини, вона вже містить мільярди клітин і починає визначатися, як пухлинна маса.
Інвазія і поширення Пухлина проростає у тканину поза базальною мембраною. Окремі пухлинні клітини проникають у новоутворену кровоносну сітку, і плином крові можуть мігрувати у інші анатомічні ділянки тіла. Пухлина вагою 1 г здатна надіслати близько 1 млн своїх клітин у кров’яне русло щоденно.
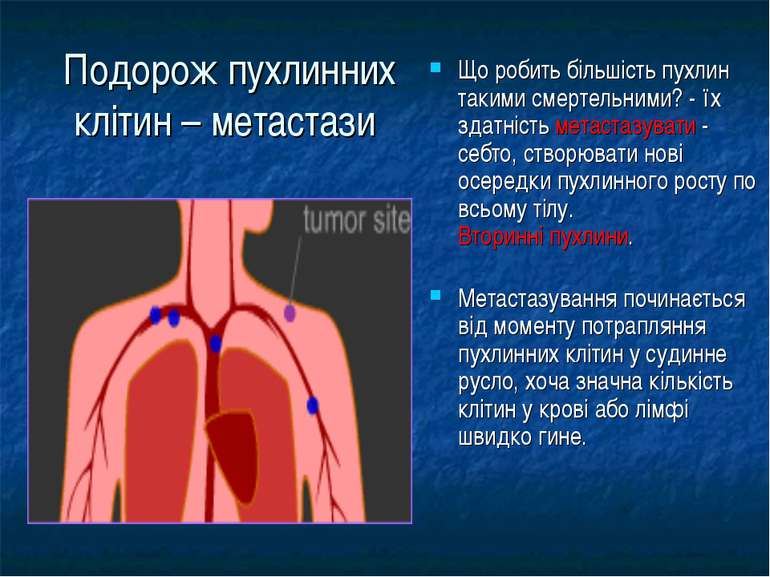
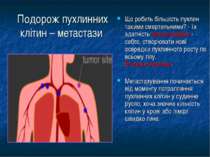
Подорож пухлинних клітин – метастази Що робить більшість пухлин такими смертельними? - їх здатність метастазувати - себто, створювати нові осередки пухлинного росту по всьому тілу. Вторинні пухлини. Метастазування починається від моменту потрапляння пухлинних клітин у судинне русло, хоча значна кількість клітин у крові або лімфі швидко гине.
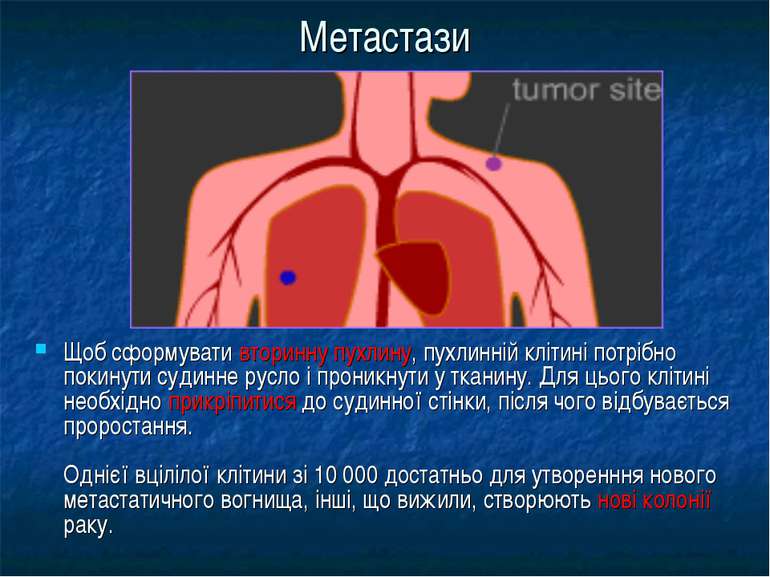
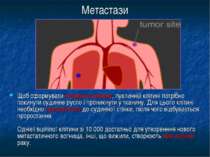
Метастази Щоб сформувати вторинну пухлину, пухлинній клітині потрібно покинути судинне русло і проникнути у тканину. Для цього клітині необхідно прикріпитися до судинної стінки, після чого відбувається проростання. Однієї вцілілої клітини зі 10 000 достатньо для утворенння нового метастатичного вогнища, інші, що вижили, створюють нові колонії раку.
Передракові захворювання – захворювання, на фоні яких можливе виникнення злоякісної пухлини Факультативний передрак – захворювання з низькою частотою можливої малігнізації (фіброаденома молочної залози, гамартрома легені, хронічний гастрит і т.д.). Облігатний передрак – захворювання з високою частотою малігнізації (поліпоз шлунково-кишкового тракту, кальозна виразка шлунка, анацидний гастрит і т.д.) .
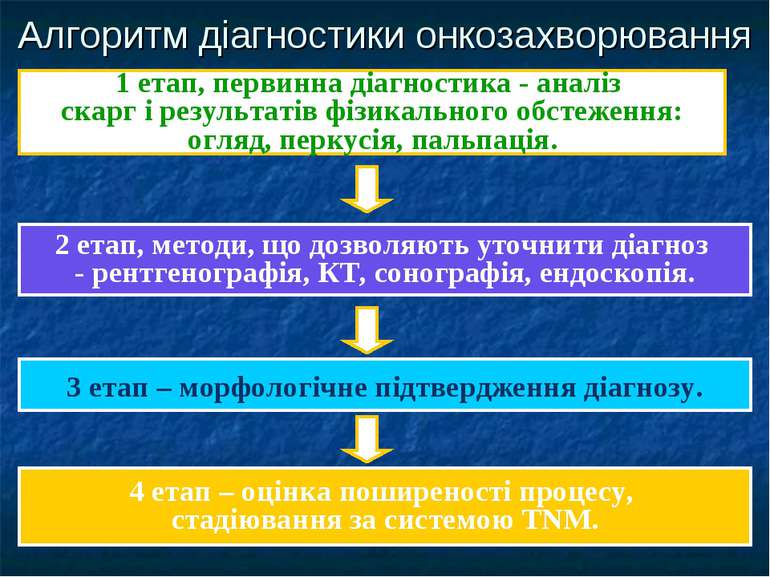
Алгоритм діагностики онкозахворювання 1 етап, первинна діагностика - аналіз скарг і результатів фізикального обстеження: огляд, перкусія, пальпація. 2 етап, методи, що дозволяють уточнити діагноз - рентгенографія, КТ, сонографія, ендоскопія. 3 етап – морфологічне підтвердження діагнозу. 4 етап – оцінка поширеності процесу, стадіювання за системою TNM.
Методи морфологічної верифікації пухлинного процесу Зішкріб з поверхні пухлини, мазок–відбиток Пункція пухлини (під рентген-, УЗД- чи КТ- контролем) Лапароскопія чи торакоскопія Ендоскопічне дослідження з біопсією Трепанбіопсія пухлини (грудної залози, м’яких тканин, кісток) Відкрита біопсія пухлини (інцизійна, ексцизійна) Інтраопераційне (термінове) морфологічне дослідження
Клінічні прояви злоякісної пухлини - паранеоплазії Паранеопластичні синдроми – різноманітні загальні порушення, які викликані пухлинним процесом, що проявляється на відстані від пухлини і метастазів. Загальні ознаки і закономірності розвитку паранеоплазій: загальні патогенетичні механізми; розвиваються при наявності злоякісних пухлин; неспецифічність клініко-лабораторних проявів; відсутність паралелізму з місцевими клінічними проявами пухлини; можливість розвитку до появи перших симптомів пухлини; резистентність до звичайних методів терапії; зникнення після радикального лікування пухлини і поява при розвитку рецидиву.
Основні патогенетичні механізми розвитку паранеоплазій Вплив біологічно активних білків, поліпептидів, факторів росту, інтерлекінів, цитокінів, простагландинів, ензимів, ембріональних протеїнів, що секретуються пухлиною. Розвиток аутоімунних процесів або імуносупресії. Утворення ектопічних рецепторів або конкурентне блокування дії гормонів біологічно неактивними гормонами, що продукуються пухлиною. «Заборонений контакт» - наявність у крові біологічно активних речовин, які відсутні в нормі. Генетично обумовлена схильність до іммуносупрессії та інші причини.
Патогенез розвитку симптомів злоякісних пухлин Основні (патогенетичні) симптоми злоякісної пухлини (по Шайну А.А.) I – факт наявності пухлини. II – місцеві симптоми: Ф – порушення функції органу; Б – больові відчуття; В – патологічні виділення. III – загальні симптоми: П – паранеоплазії, І – інтоксикація. IV – симптоми ускладнень і метастазів.
Лікування онкологічних хворих Радикальним вважається таке лікування, коли після його проведення не залишається вогнищ пухлинного росту. Паліативним називають таке лікування, коли після його проведення залишаються неліквідовані вогнища пухлини як в зоні розташування первинного вогнища так і у віддалених органах. Симптоматичне лікування передбачає усунення ускладнень, які загрожують життю хворого на рак.
Спеціалізоване лікування Основні методи – хірургічне - променева терапія - хіміотерапія Додаткові методи – гормонотерапія - імунотерапія
Національний план боротьби з раком Профілактика Скринінг і раннє розпізнавання Допомога онкологічним хворим Навчання фахівців Наукові дослідження та контроль за онкоепідеміологічною ситуацією в країні
Профілактика За даними Міжнародної Асоціації у Боротьбі з Раком близько 80% усіх видів раку зумовлені зовнішніми чинниками, а отже потенційно можуть бути попереджені (IARC, 2003).
Профілактика – реальна перспектива вирішення проблеми раку Первинна профілактика раку: боротьба з курінням, пропаганда правильного харчування і здорового способу життя - дозволяє зменшити захворюваність в 1,5-2 рази. Вторинна профілактика – виявлення і лікування передракових захворювань, скринінгові програми по виявленню передраку і ранніх форм раку: УЗД і мамографія у жінок, тест на скриту кров при колоректальному раку, цитологічний скринінг раку шийки матки, ендоскопічний скринінг раку шлунка – дозволяє перевести ці захворювання до виліковних. Індивідуальна профілактика раку, базується на виявленні спадкових генетичних дефектів (несприятливий фенотип зустрічається у 40-50 % населення).
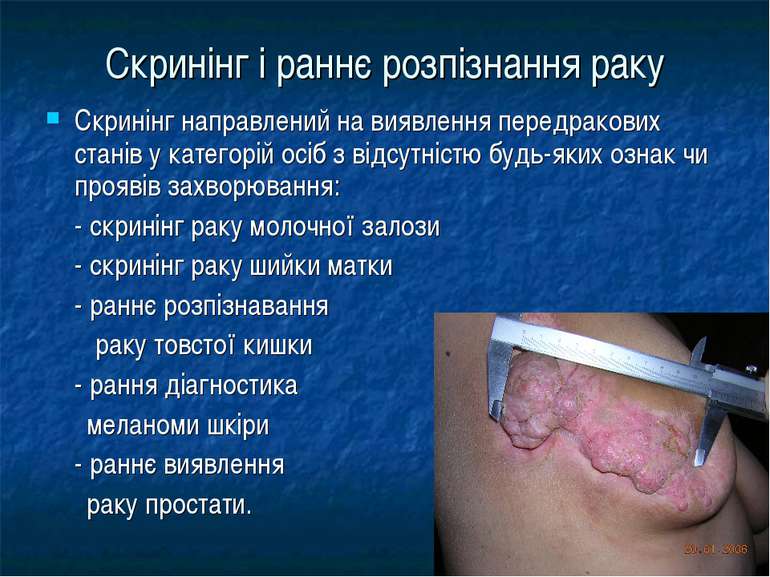
Скринінг і раннє розпізнання раку Скринінг направлений на виявлення передракових станів у категорій осіб з відсутністю будь-яких ознак чи проявів захворювання: - скринінг раку молочної залози - скринінг раку шийки матки - раннє розпізнавання раку товстої кишки - рання діагностика меланоми шкіри - раннє виявлення раку простати.
Допомога онкологічним хворим діагностика та лікування психологічна допомога реабілітація та диспансерний нагляд соціальний захист та інформаційна підтримка пацієнтів паліативна допомога
Основу ранньої діагностики визначає рівень онкологічної настороженості, яка включає: знання ранніх симптомів раку; знання клініки, діагностики, диспансеризації і лікування хворих з передраковими станами; знання принципів організації онкодопомоги та цілеспрямоване направлення хворого в онкологічний заклад; ретельне всебічне обстеження кожного, хто звернувся в лікувальний заклад (проведення обов’язкового клінічного мінімуму обстежень); у всіх випадках так званої трудної діагностики установка на первинне виключення у хворого раку.
Обов’язковий клінічний мінімум обстеження: Збір анамнезу за системами з метою виявлення ознак порушення функції органів, а також факторів ризику для виникнення раку, з подальшим поглибленим (комплексним) обстеженням органів і систем, які мають найбільший зв’язок з виявленими ФР і симптомами. Огляд шкіри, слизових, периферичних лімфатичних вузлів, методичне обстеження грудних залоз; в оглядовому кабінеті для чоловіків – огляд і промацування зовнішніх статевих органів і пальцеве дослідження прямої кишки з метою виявлення патології простати і дистальних відділів прямої кишки; в оглядовому кабінеті для жінок – вагінальне дослідження із забором мазків з шийки матки, а також ректальне дослідження. Тут також проводиться огляд грудних залоз. Флюорографія ОГК в трьох проекціях. Аналіз крові і сечі. УЗД печінки, нирок, матки і додатків
Схожі презентації
Категорії