Презентація на тему:
Означення загальної характеристики основ
Завантажити презентацію
Означення загальної характеристики основ
Завантажити презентаціюПрезентація по слайдам:
Тема: “Загальна характеристика основ”. 8кл. Учитель хімії Верховцевського НВК Кукса Наталія Миколаївна Україна. Дніпропетровська область.
Мета уроку: 1. Познайомити учнів з новим класом неорганічних сполук – основами. 2. Розглянути класифікацію, склад та номенклатуру основ. 3.Фізичні та хімічні властивості 4. Зстосування основ в побуті
Будова основ та їх назви Класифікація Фізичні властивості Хімічні властивості Застосування в побуті та промисловості Правила поводження з лугами
2. Цей оксид складає 80 % маси клітини всього живого та виконує в ній дуже важливі функції: CO2 H2O CaO NH3 - - + -
5. Дана сполука використовуєтьсятся для приготування шипучих напоїв: - + - HCl CaO CO2 NH3 -
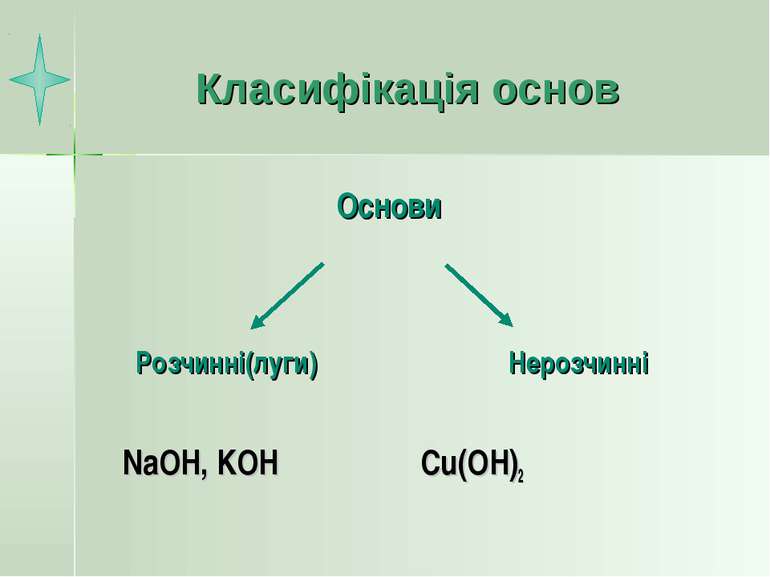
Основи – це складні речовини, в яких йони металів з’єднані з одною чи декільками гідроксид-йонами.
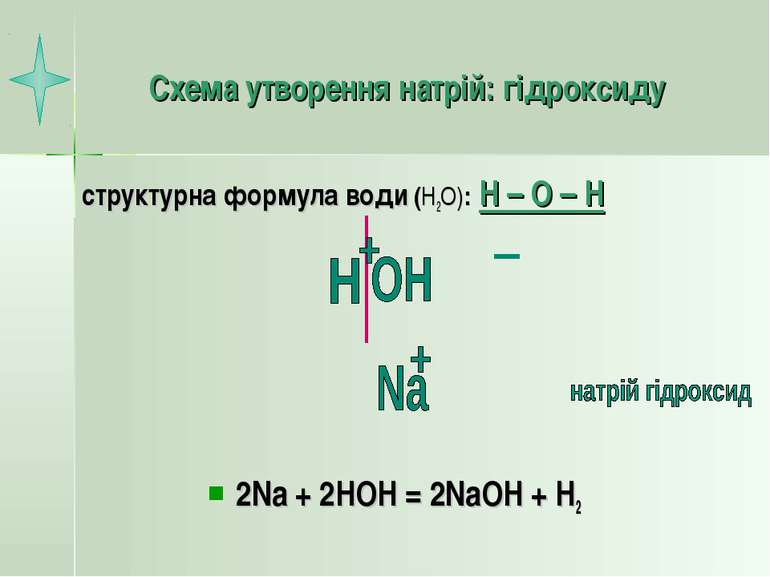
Схема утворення натрій: гідроксиду структурна формула води (Н2О): Н – О – Н 2Na + 2HOH = 2NaOH + H2
Оксидам металів відповідають основи: Складіть основи з оксидів: ZnO, Li2O, MgO. Спробуйте самостійно скласти оксиди з основ: CuOH, Cu(OH)2
Номенклатура: Ca(OH)2 –кальций гідроксид Fe(OH)2 – ферум (ІІ) гідроксид Fe(OH)3 – ферум (ІІІ) гідроксид Zn(OH)2 Al(OH)3 Cu(OH)2 CuOH Слово гідро ксид метал Валент ність
Фізичні властивості основ: Тверді,кристалічні Ті,що утворюються під час реакцій Луги(розчинні) дуже їдкі Мають різні кольори
Взаємодіють з кислотами KOH+HCl= KCl+H2O Взаємодіють з кислотними оксидами 2KOH+CO2 =K2CO3+H2O Взаємодіють з солями KOH+NaCl=KCl+NaOH Нерозчинні розкладаються при нагріванні Сu(OH)2=CuO+H2O
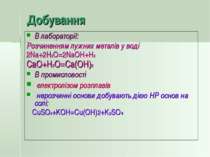
Добування В лабораторії: Розчиненням лужних металів у воді 2Na+2H2O=2NaOH+H2 CaO+H2O=Ca(OH)2 В промисловості електролізом розплавів нерозчинні основи добувають дією НР основ на солі: СuSO4+KOH=Cu(OH)2+K2SO4
Застосування NaOH – для виробництва мила,ліків, в текстильній промисловості, очищування нафти. KOH - в аккумуляторах. Ca(OH)2 (гашене вапно)– у виробництві цукру, соди, в будівництві, для приготування бордоської суміші – засобу для боротьби з хворобами та шкідниками рослин.
Схожі презентації
Категорії




























































![Звуки [б][б’], позначення їх буквою «бе». Звуко-буквений аналіз слів Звуки [б][б’], позначення їх буквою «бе». Звуко-буквений аналіз слів](/images/1/880/210/img0.jpg)
![Звуки [з],[з’].Позначення їх буквами «З», «з»(зе) Звуки [з],[з’].Позначення їх буквами «З», «з»(зе)](/images/1/881/210/img0.jpg)
![Звуки [ц],[ц’]. Позначення їх буквами Ц,ц(«це») Звуки [ц],[ц’]. Позначення їх буквами Ц,ц(«це»)](/images/2/1139/210/img0.jpg)



















